Aldolkondensation
En aldolkondensation er en organisk reaktion hvor en enol eller en enolat ion reagerer med en carbonyl og danner em β-hydroxyaldehyd eller β-hydroxyketon, efterfulgt af en dehydrering og giver en konjugeret enon.

Aldolkondensationer er vigtige i organisk syntese, da de er en god måde at lave carbon-carbon-bindinger. Eksempelvis benytter Robinson annulation reaktionen, som kan danne en Wieland-Miescher keton, der er et vigtigt stof i mange organiske synteser. Aldolkondensationer bruges ofte i universitetssammenhænge inden for organisk kemi som et vigtigt eksempel på en reaktionsmekanisme.[1][2][3] I dens normale form involverer den en nukleofil addition af en keton-enolat til en aldehyd for at danne en β-hydroxyketon, eller "aldol" (aldehyd + alcohol), en strukurel enhed der findes i mange naturligt forekommende molekyler og lægemidler.[4][5][6]
Navnet aldolkondensation bruges almindeligvis, særligt inden for biokemi, til at referere til den første del af reaktionen (additionen). Aldolreaktionen selv bliver katalyseres af aldolase. Formelt set er aldolreaktionen ikke en kondensationsreaktion, da den ikke involverer tabet af et lille molekyle.
Reaktionen mellem en aldehyd/keton og en carbonyl, der mangler et alpha-hydrogen (krydsaldolkondensation) kaldes en Claisen-Schmidt kondensation. Denne reaktion er opkaldt efter de to kemikere Rainer Ludwig Claisen og J. G. Schmidt, der uafhængigt af hinanden udgav videnskabelige artikler om emnet i 1880 og 1881.[7][8][9] Et eksempel på er syntesen af dibenzylidenacetone.
Mekanisme[redigér | rediger kildetekst]
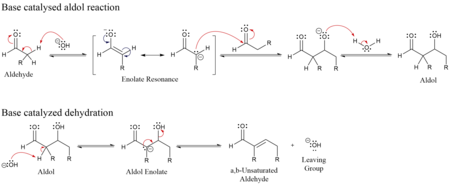
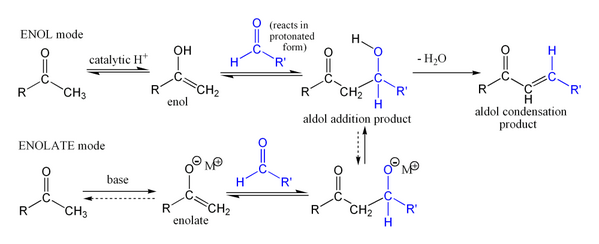
Den første del af reaktionen er en aldolreaktion, og den anden del er en dehydrering -, en eliminationsreaktion der involverer dannelsen af vand eller en alkohol. Dehydreringen kan ske sammen med en decarboxylation, hvis der er en aktiv carboxylgruppe til stede. Aldoladditionsproduktet kan blive dehydreret via to mekanisme; en stærk base som kalium-t-butoxide, kaliumhydroxid eller natriumhydrid i en enolatmekanisme,[10] eller i en syrekatalyseret enolmekanisme.

|
|
| Animation af den basekatalyserede reaktion. | Animation af den syrekatalyserede reaktion. |
Kondensationstyper[redigér | rediger kildetekst]
Det er vigtigt at skelne mellem aldolkondensationen fra andre typer additionsreaktioner til carbonyler.
- Når basen er en amin og carbanionen bliver aktiveret kaldes det en Knoevenagel kondensation.
- I en Perkinreaktion er aldehydet en aromatisk forbindelse og enolaten dannes fra et anhydrid.
- En Claisen-kondensation involverer to estere.
- En Dieckmann-kondensation involverer to estergrupper i det samme molekyle og danner et cyklisk molekyle.
- En Henryreaktion involverer et aldehyd og en alifatisk nitroforbindelse.
- En Robinson annulation involverer en α,β-umættet keton og en carbonylgruppe, der først laver en Michaelreaktion inden aldolkondensationen.
- I Guerbetreaktionen dannes et aldehyd in situ fra en alkohol, der selvkondenserer til den dimeriserede alkohol.
- I Japp–Maitland kondensationen bliver vand ikke fjernet ved en eliminationsreaktion, men ved en nukleofil udskiftning
Aldox proces[redigér | rediger kildetekst]
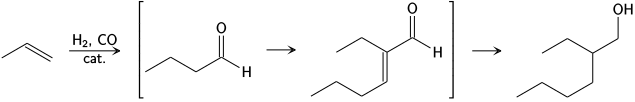
I industrien blev Aldox processen udviklet af Royal Dutch Shell og Exxon, der omdanner propylen og syntesegas direkte til 2-Ethylhexanol via hydroformylation til butyraldehyde, aldolkondensation til 2-ethylhexenal og til sidst en hydrogenering.[11]
Det er også lykkedes at omdanne crotonaldehyd direkte til 2-ethylhexanal i et system bestående af palladium, Amberlyst og superkritisk kuldioxid:[12]
Se også[redigér | rediger kildetekst]
Referencer[redigér | rediger kildetekst]
- ^ Wade, L. G. (2005). Organic Chemistry (6th udgave). Upper Saddle River, NJ: Prentice Hall. s. 1056–1066. ISBN 0-13-236731-9.
- ^ Smith, M. B.; March, J. (2001). Advanced Organic Chemistry (5th udgave). New York: Wiley Interscience. s. 1218–1223. ISBN 0-471-58589-0.
{{cite book}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Mahrwald, R. (2004). Modern Aldol Reactions. Vol. 1, 2. Weinheim, Germany: Wiley-VCH. s. 1218-1223. ISBN 3-527-30714-1.
- ^ Heathcock, C. H. (1991). Additions to C-X π-Bonds, Part 2. Comprehensive Organic Synthesis. Selectivity, Strategy and Efficiency in Modern Organic Chemistry. Vol. 2. Oxford: Pergamon. s. 133-179. ISBN 0-08-040593-2.
- ^ Mukaiyama T. (1982). "The Directed Aldol Reaction". Organic Reactions. 28: 203-331. doi:10.1002/0471264180.or028.03.
- ^ Paterson, I. (1988). "New Asymmetric Aldol Methodology Using Boron Enolates". Chemistry and Industry. London: Paterson Group. 12: 390-394.
- ^ Claisen, L.; Claparède, A. (1881). "Condensationen von Ketonen mit Aldehyden". Berichte der Deutschen Chemischen Gesellschaft. 14 (1): 2460-2468. doi:10.1002/cber.188101402192.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Schmidt, J. G. (1881). "Ueber die Einwirkung von Aceton auf Furfurol und auf Bittermandelöl in Gegenwart von Alkalilauge". Berichte der Deutschen Chemischen Gesellschaft. 14 (1): 1459-1461. doi:10.1002/cber.188101401306.
- ^ March, J. (1985). Advanced Organic Chemistry: Reactions, Mechanisms and Structure (3rd udgave). Wiley Interscience. ISBN 0-471-85472-7.
- ^ Nielsen, A. T.; Houlihan., W. J. (1968). "The Aldol Condensation". Organic Reactions. 16: 1-438. doi:10.1002/0471264180.or016.01.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Foreksempel BG 881979
- ^ Seki, T.; Grunwaldt, J.-D.; Baiker, A. (2007). "Continuous catalytic "one-pot" multi-step synthesis of 2-ethylhexanal from crotonaldehyde". Chemical Communications. 2007 (34): 3562-3564. doi:10.1039/b710129e.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link)