Hess' lov
Hess' Lov er en lov inden for den fysiske kemi, der blev fremsat af Germain Henri Hess i 1840. Hess' lov anvendes til at forudsige entalpiændringer for kemiske reaktioner.
Loven[redigér | rediger kildetekst]
Ifølge loven kan entalpiændringen for en reaktion beregnes, hvis den kan deles op i delreaktioner med kendte entalpiændringer. Entalpien er således uafhængig af vej og dermed en tilstandsfunktion.
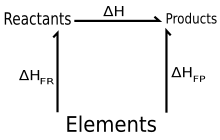
Som et udbredt specialtilfælde af loven, kan dannelsesentalpien for produkterne og reaktanterne bruges. Dannelsesentalpien er entalpiændringen, hvis reaktanterne er grundstoffer. For en generel reaktion
er entalpiændringen altså givet ved
hvor den samlede dannelsesentalpi for reaktanterne trækkes fra produkternes dannelsesentalpi.[1]
Kildehenvisninger[redigér | rediger kildetekst]
- ^ Atkins, Peter; de Paula, Julio (2006), "2: The First Law", Atkins' Physical Chemistry (8. udgave), Oxford University Press, s. 53-55, ISBN 9780198700722
| | Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |




