Tryptophan: Forskelle mellem versioner
Danielle (diskussion | bidrag) Ændrer fra redirect |
exchanged image (PNG -> SVG) |
||
| Linje 1: | Linje 1: | ||
{{kemiboks ny |
{{kemiboks ny |
||
| BilledFil = Tryptophan - Tryptophan. |
| BilledFil = Tryptophan - Tryptophan.svg |
||
| Section1 = {{Kemiboks Generelt |
| Section1 = {{Kemiboks Generelt |
||
| IUPACNavn = (''S'')-2-Amino-3-(1H-indol-3-yl)-<br>propansyre |
| IUPACNavn = (''S'')-2-Amino-3-(1H-indol-3-yl)-<br>propansyre |
||
Versionen fra 6. feb. 2007, 01:03
| Tryptophan | |
|---|---|
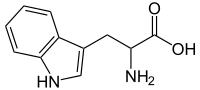
| |
| Generelt | |
| Systematisk navn | (S)-2-Amino-3-(1H-indol-3-yl)- propansyre |
| Molekylformel | C11H12N2O2 |
| Molmasse | 204,23 g/mol |
| CAS nummer | [73-22-3] |
| SMILES | C(N)(C(=O)O)CC1c2ccccc2NC=1 |
| Egenskaber | |
| Massefylde | 1,34 g cm |
| Smeltepunkt | 289 °C |
| Syrestyrkekonstant (pKa) | 2,38 |
| Basestyrkekonstant (pKb) | 9,34 |
| Isoelektrisk punkt (pI) | 5,89 |
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |
Tryptophan (også Trp eller W) er en essentiel aminosyre. Den findes i to isomere former, en L- og en D-form, hvoraf kun den ene (L-formen) findes i pattedyr. D-formen findes af og til i naturlige materialer, f.eks. i det giftige peptid contryphan.
Tryptophan er startmolekyle i syntesen af serotonin (en neurotransmitter), melatonin (et neurohormon) og niacin. Tryptophans funktionelle gruppe er en indol.
Der sidder ofte tryptophanrester i membranproteiner tæt ved grænsefladen mellem membranens hydrofobe indre og det vandige omgivende miljø. Disse rester hjælper til med at forankre proteinerne i membranen. Tryptophans aromatiske ring er fluorescerende, hvilket ofte udnyttes i studier af proteiners foldning.
Tryptophan findes i store mængder i bananer, mælk, jogurt, hytteost, rødt kød, fisk, fjerkræ, sesamfrø, solsikkerkerner, græskarkerner og jordnødder.
