Radikal (kemi): Forskelle mellem versioner
Content deleted Content added
EmausBot (diskussion | bidrag) m r2.7.2+) (Robot tilføjer be:Свабодныя радыкалы |
EmausBot (diskussion | bidrag) m r2.7.3) (Robot ændrer uk:Замісник (хімія) |
||
| Linje 51: | Linje 51: | ||
[[sv:Fri radikal]] |
[[sv:Fri radikal]] |
||
[[th:อนุมูลอิสระ]] |
[[th:อนุมูลอิสระ]] |
||
[[uk: |
[[uk:Замісник (хімія)]] |
||
[[vi:Gốc tự do]] |
[[vi:Gốc tự do]] |
||
[[zh:自由基]] |
[[zh:自由基]] |
||
Versionen fra 17. sep. 2012, 22:17
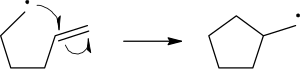
I kemi er et radikal eller et frit radikal betegnelsen for et atom eller en forbindelse som har en uparret elektron eller en ufuldstændig fyldt elektronskal. De uparrede elektroner er meget reaktive, og radikaler deltager derfor nemt i kemiske reaktioner. Radikaler har ingen ladning og deres reaktivitet er derfor ofte anderledes end lignende ioner.
Radikaler spiller en vigtig rolle i atmosfærekemi, polymerisering, blodplasmakemi og biokemi.
Frie radikaler kan opstå som et resultat af ultraviolet lys fra solen, ozon, radioaktiv stråling, tobaksrøg, luftforurening osv., og kan i sidste ende være en vigtig faktor i udviklingen af kræft. Det eneste kendte middel mod de frie radikaler, er antioxidanter.
| | Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
