Influenza
| Influenza | |
|---|---|
 | |
| Specialità | medicina generale, pneumologia, infettivologia e medicina d'emergenza-urgenza |
| Eziologia | Orthomyxoviridae |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 487 |
| ICD-10 | J10, J11 e J9 |
| OMIM | 614680 |
| MeSH | D007251 |
| MedlinePlus | 000080 |
| eMedicine | 219557 e 972269 |
L’influenza è una malattia infettiva respiratoria acuta causata dal virus dell'influenza, un virus a RNA della famiglia degli Orthomyxoviridae[1]. I sintomi possono essere da lievi a severi; i più comuni sono febbre, faringodinia (mal di gola), coriza, rinorrea (naso che cola), mialgie e artralgie (dolori ai muscoli e alle articolazioni), cefalea, tosse e malessere generale. Tipicamente i sintomi iniziano due giorni dopo l'esposizione al virus (periodo di incubazione) e generalmente durano meno di una settimana.
La tosse può durare anche più di due settimane. Nei bambini ci può essere nausea e vomito, che in realtà non sono comuni nell'adulto. La nausea e il vomito sono presenti più comunemente in infezioni gastroenteriche non correlate al virus dell'influenza, che a volte, in maniera inappropriata, sono chiamate “influenza intestinale”.[2] La malattia può colpire anche le vie respiratorie basse. Le complicanze dell'influenza includono la polmonite virale, la polmonite batterica secondaria, l'infezione dei seni paranasali, il peggioramento di problemi di salute preesistenti, come l'asma e lo scompenso cardiaco[3].
Tre tipi di virus dell'influenza infettano l'uomo: sono chiamati Tipo A, Tipo B e Tipo C. Di solito il virus è trasmesso per via aerea con la tosse o gli starnuti: ciò si ritiene che accada per lo più a distanza relativamente ravvicinata. L'influenza può essere spesso trasmessa toccando superfici contaminate dal virus e poi portandosi le mani alla bocca e agli occhi[4]. Il periodo di contagiosità inizia un giorno prima della comparsa dei sintomi e termina circa una settimana dopo; bambini e persone immunodepresse possono essere contagiose per un periodo più lungo[5]. L'infezione può essere confermata cercando il virus nelle secrezioni della gola, del naso, delle vie aeree più basse (espettorato) e nella saliva. Il test più accurato è la ricerca dell'RNA virale con PCR (polymerase chain reaction).
Il frequente lavaggio delle mani riduce il rischio di infezione poiché il virus è inattivato dal sapone[6]. È anche utile indossare una mascherina chirurgica. La vaccinazione annuale contro l'influenza è raccomandata dall'Organizzazione mondiale della sanità per i soggetti ad elevato rischio.
Il vaccino è di solito efficace contro tre o quattro tipi di influenza ed è usualmente ben tollerato. Il vaccino preparato per un anno può non essere utile nell'anno successivo, dal momento che il virus evolve rapidamente. Sono stati utilizzati alcuni farmaci antivirali come l'inibitore della neuraminidasi oseltamivir per trattare l'influenza. I loro benefici in persone per altri aspetti sane non appaiono superare i loro rischi[7]. Non sono stati trovati benefici anche nei pazienti con altre patologie[8].
L'Organizzazione mondiale della sanità ha dichiarato l'epidemia di un nuovo tipo di influenza A/H1N1 come una pandemia nel giugno 2009[9].
L'influenza può anche colpire altri animali come il maiale, il cavallo e alcuni uccelli[10].
Storia[modifica | modifica wikitesto]
Il nome di questa infezione deriva dalla vecchia concezione astrologica e della dottrina miasmatico-umorale di questa malattia, che affermava che la malattia fosse causata dall’influenza degli astri.
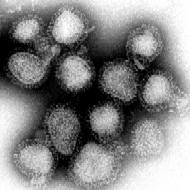
I sintomi dell'influenza umana furono descritti da Ippocrate circa 2400 anni fa[11][12]. Da allora, il virus ha causato diverse pandemie. I dati storici sono difficili da interpretare, poiché i sintomi possono essere simili a quelli di altre malattie come difterite, febbre tifoide o dengue. La parola "influenza" venne introdotta all'inizio del Quattrocento in Italia per descrivere un'epidemia causata dall'influenza degli astri; lo stesso termine venne accolto nella lingua inglese nel Settecento, mentre i francesi chiamarono la malattia con il nome di grippe.[13] La prima registrazione certa di una pandemia di influenza risale al 1580, quando il virus si sviluppò in Asia e si sparse in Europa attraverso l'Africa. La mortalità era elevata anche a causa dell'abitudine di effettuare salassi. Nella Roma del Rinascimento circa 8000 persone perirono e gravi focolai si ebbero in molte città spagnole. La pandemia continuò sporadicamente attraverso il XVII ed il XVIII secolo, e nel 1830-1833 fu particolarmente estesa, infettando circa un quarto della popolazione esposta[14].
La più famosa e letale pandemia fu la cosiddetta "influenza spagnola"[15] (influenza di tipo A, sottotipo H1N1), che comparve dal 1918 al 1919. La denominazione fu impropria, dato che le tracce storiche attribuiscono ad altri luoghi l'apparizione dei primi casi, vedi l'ondata epidemica cinese nel marzo 1918 oppure quella tra le truppe statunitensi in servizio nel Kansas.[13] Stime successive indicarono da 40 a 50 milioni di vittime[16], mentre stime attuali indicano un numero variabile tra 50 e 100 milioni di persone uccise dal virus[17]. Questa pandemia è stata descritta come "il più grande olocausto medico della storia", e potrebbe aver ucciso tante persone quante ne fece la peste nera[14]. Questo terribile numero di vittime venne causato da un tasso di infezione estremamente elevato (superiore al 50%) e l'estrema gravità dei sintomi, causati forse da una "tempesta citochinica"[16]. Infatti i sintomi nel 1918 erano talmente inusuali che inizialmente venne diagnosticata come dengue, colera o tifo. Un osservatore scrisse: "Una delle complicazioni più impressionanti è l'emorragia dalle membrane delle mucose, specialmente il naso, lo stomaco e l'intestino. Può accadere anche il sanguinamento dalle orecchie o da petecchie emorragiche sulla pelle"[17]. La maggioranza delle morti avvenne a causa di polmonite batterica, una infezione secondaria provocata dall'influenza, ma il virus uccise anche direttamente, causando emorragie massive ed edemi polmonari[18].
L'influenza spagnola fu veramente globale, estendendosi addirittura fino all'Artide e alle isole remote del Pacifico. Questa malattia insolitamente grave uccise tra il 2% e il 20% degli infetti (il rapporto tra contagi letali e contagi totali diagnosticati è detto "tasso di letalità" o, in inglese, Case Fatality Ratio - da non confondersi con il tasso di mortalità), a differenza delle normali epidemie di influenze che si aggira attorno allo 0,1%[15][17].
Un'altra strana caratteristica della pandemia era costituita dalla letalità molto elevata in giovani adulti, in quanto il 99% dei decessi totali fu di persone con meno di 65 anni, e più della metà delle morti tra adulti dai 20 ai 40 anni[19]. Questa caratteristica è strana poiché l'influenza è normalmente più letale in persone molto giovani (sotto i 2 anni) e molto anziane (oltre i 70 anni). La mortalità totale della pandemia non è nota, ma è stimata tra il 2,5% e il 5% della popolazione mondiale. 25 milioni di persone potrebbero essere morte nelle prime 25 settimane. In paragone l'AIDS ha ucciso 25 milioni di persone nei primi 25 anni[17].
Verso la fine dell'Ottocento si diffuse il modello microbiologico di spiegazione per le malattie infettive ed in quegli anni venne scoperto il bacillo Haemophilus influenzae grazie alle ricerche del batteriologo tedesco Richard F.J. Pfeiffer e per molti anni fu considerata questa la causa dell'epidemia; solamente negli anni venti il virus fu isolato nei maiali e salì alla ribalta la reale causa virale dell'influenza. Altri studi degni di nota furono quelli portati avanti da Richard E. Shope nel 1931 che dimostrò la trasmissibilità del virus tra i maiali usando materiale filtrato estratto dalle vie respiratorie di maiali malati; nel 1933 Wilson Smith riuscì ad indurre la polmonite nei topi grazie all'inoculazione di materiale infetto preso dal naso dei furetti; nel 1940 i furetti vennero infettati con un secondo ceppo virale proveniente da esseri umani, che fu definito "influenza B", mentre nel 1949 fu isolato un terzo ceppo influenzale definito "C". Nel 1940 l'australiano F.M.Burnet fece una scoperta che aprì le porte alla preparazione dei vaccini, quando notò che i virus influenzali si moltiplicavano nell'embrione del pollo.[13]
Le successive pandemie di influenza non furono così devastanti. L'influenza asiatica del 1957 (tipo A, ceppo H2N2) e l'influenza di Hong Kong del 1968 (tipo A, ceppo H3N2) furono minori, anche se morirono milioni di persone. Nel 1977 l'influenza russa morirono circa 0,7 milioni di persone.[20][21] Nelle ultime pandemie erano disponibili gli antibiotici per il controllo delle infezioni secondarie che contribuirono a ridurre la mortalità, a differenza della influenza spagnola del 1918[15].
| Pandemia | Data | Decessi | Sottotipo | Indice di gravità della pandemia (Pandemic Severity Index)[23]. | Tasso di letalità associato (intervallo) |
|---|---|---|---|---|---|
| Asiatica (russa) | 1889–1890 | 1 milione | forse H2N2 | 3 | <1% |
| Spagnola | 1918–1920 | da 40 a 100 milioni | H1N1 | Categoria 5 | >2% |
| Asiatica | 1957–1958 | da 1 a 4 milioni[24] | H2N2 | Categoria 2 | 0,1% - 0,5% |
| Hong Kong | 1968-1969 | da 1 a 4 milioni[24] | H3N2 | Categoria 2 | <0,2% |
| Russa | 1977-1979 | 0.7 milioni | H1N1 | - | |
| Suina | 2009–? | migliaia | H1N1 | Categoria 1 | meno di 0,1% |
La causa eziologica dell'influenza, i virus della famiglia Orthomyxoviridae, venne scoperta per la prima volta da Richard Schope nel 1931 nei maiali[25]. Questa scoperta venne seguita dall'isolamento del virus nell'uomo da un gruppo di ricercatori guidato da Patrick Laidlaw al Medical Research Council in Inghilterra nel 1933[26]. Tuttavia, solo quando nel 1935 Wendell Stanley per la prima volta studiò il virus del mosaico del tabacco venne compresa la natura non cellulare dei virus.
Il primo passo significativo nella prevenzione dell'influenza fu lo sviluppo nel 1944 di un vaccino per l'influenza da parte di Thomas Francis, Jr., basandosi sul lavoro di Frank Macfarlane Burnet, che dimostrò la perdita di virulenza del virus quando veniva coltivato in uova di gallina fertilizzate[27]. L'applicazione delle osservazioni da parte di Francis permise al gruppo di ricercatori all'Università del Michigan di sviluppare il primo vaccino influenzale, con il supporto dell'esercito statunitense[28]. L'esercito venne profondamente coinvolto nella ricerca a causa dell'esperienza nella prima guerra mondiale, quando migliaia di soldati furono uccisi dal virus in pochi mesi[17].
Anche se ci furono delle preoccupazioni nello stato del New Jersey nel 1976, a livello mondiale nel 1977 e in nazioni asiatiche nel 1997, non ci furono pandemie dopo l'influenza di Hong Kong del 1968. L'immunità ai ceppi di influenza delle precedenti pandemie e la vaccinazione hanno limitato la diffusione del virus e potrebbero aver aiutato nella prevenzione di ulteriori pandemie[22].
Ricerca scientifica[modifica | modifica wikitesto]

Le ricerche sull'influenza includono gli studi sulla virologia molecolare, sul come il virus produce malattie (patogenesi), la risposta immunitaria dell'ospite, la genetica virale e come si propaga il virus (epidemiologia). Questi studi aiutano lo sviluppo di contromisure, ad esempio una migliore comprensione della risposta immunitaria aiuta lo sviluppo del vaccino e la comprensione del meccanismo con cui il virus invade le cellule aiuta lo sviluppo di farmaci antivirali. Un importante programma di ricerca è l’Influenza Genome Sequencing Project, che sta creando una libreria di sequenze, che dovrebbe aiutare a chiarire quali fattori rendono un ceppo più letale di un altro, quali geni sono più coinvolti nelle immunità e come il virus evolve nel tempo[29].
La ricerca di nuovi vaccini è particolarmente importante: i vaccini attuali sono lenti e costosi da produrre e devono essere riformulati ogni anno. Il sequenziamento del genoma dell'influenza e le tecnologia a DNA ricombinante possono accelerare la generazione di nuovi ceppi di vaccini permettendo agli scienziati di sostituire in nuovi antigeni in ceppi di vaccini già esistenti[30]. Le nuove tecnologie che sono in sviluppo per la crescita del virus in una coltura cellulare promettono rese maggiori, costi inferiori, qualità migliore[31]. Le ricerche su un vaccino universale per l'influenza A, mirato contro la protenina M2 sono in corso alla university of Ghent da Walter Fiers e il suo team[32][33][34].
Epidemiologia[modifica | modifica wikitesto]
Variazioni stagionali[modifica | modifica wikitesto]
Il picco influenzale avviene in inverno, e poiché nell'emisfero boreale e in quello australe l'inverno giunge in periodi dell'anno diversi, esistono due diverse stagioni influenzali ogni anno. Per questo motivo l'OMS raccomanda due diverse formulazioni di vaccino ogni anno, una per il nord e una per il sud[35].
Non è totalmente chiaro il motivo dell'insorgenza stagionale di focolai influenzali, invece di un'insorgenza uniforme durante tutto l'anno. Una possibile spiegazione è che, poiché le persone passano maggiormente il tempo in luoghi chiusi durante l'inverno, esse sono in contatto più spesso, e questo promuove la trasmissione da persona a persona. Un'altra spiegazione si basa sulle basse temperature che comportano un'aria più secca che può deidratare le mucose e impedire che il corpo possa espellere efficacemente le particelle di virus. Il virus potrebbe anche sopravvivere più a lungo su superfici esposte a temperature più basse. Inoltre l'aumento dei viaggi dovuto alle vacanze invernali può giocare a favore del virus[36]. Un fattore importante è costituito dall'elevata trasmissione tramite aerosol del virus in ambienti freddi (con temperature inferiori ai 5 °C) con bassa umidità[37]. Tuttavia cambiamenti stagionali nel tasso di infezioni avvengono anche nelle regioni tropicali, e i picchi di infezione avvengono principalmente durante la stagione delle piogge[38]. Le modifiche stagionali nei contatti tra persone in ambiente scolastico, che costituiscono il fattore principale in altre malattie infantili come il morbillo e la pertosse possono essere significative anche nel caso dell'influenza. La combinazione di questi effetti stagionali può essere amplificato dalla "risonanza dinamica" con i cicli di malattie endogene[39]. Il ceppo H5N1 presenta carattere stagionale sia nell'uomo che nei volatili[40].
In alternativa è stato ipotizzato che le infezioni stagionali di influenza sono un effetto dei livelli di vitamina D sull'immunità al virus[41]. Quest'idea venne proposta per la prima volta nel 1965 da Robert Edgar Hope-Simpson[42]. Egli propose che la causa delle epidemie di influenza durante l'inverno potrebbero essere connesse con le fluttuazioni stagionali dei livelli di vitamina D, che è prodotta dalla pelle sotto l'influenza delle radiazioni ultraviolette del sole (o da fonti artificiali).
Questo potrebbe spiegare il motivo dell'insorgenza del virus in inverno e durante la stagione delle piogge, quando le persone passano il tempo principalmente in casa, e il loro livello di vitamina D cala. Inoltre alcuni studi hanno suggerito che la somministrazione di olio di fegato di merluzzo, che contiene grandi quantità di vitamina D, può ridurre l'incidenza di infezione del tratto respiratorio[43].
Diffusione epidemica e pandemica[modifica | modifica wikitesto]
Essendo l'influenza causata da una moltitudine di specie e ceppi di virus, ogni anno alcuni ceppi possono estinguersi mentre altri possono causare epidemie ed altri anche pandemie. Tipicamente nelle due normali stagioni influenzali in un anno (una per emisfero) ci sono tra i tre e i cinque milioni di casi di malesseri gravi e fino a 500 000 decessi a livello mondiale, che per alcune definizioni costituiscono una epidemia influenzale ogni anno[44]. Anche se l'incidenza del virus può variare molto, ogni anno, circa 36 000 decessi e più di 200 000 ospedalizzazioni sono da collegare, negli Stati Uniti, all'influenza[45][46][47].
Impatto economico[modifica | modifica wikitesto]
L'influenza causa dei costi diretti conseguenti alla perdita di produttività e ai trattamenti medici relativi, assieme a costi indiretti per le misure preventive. Negli Stati Uniti, l'influenza ha un costo di oltre 10 miliardi di dollari l'anno, e una pandemia potrebbe far aumentare i costi diretti e indiretti fino a centinaia di miliardi di dollari[48]. Tuttavia, l'impatto economico delle pandemie passate non è stato studiato e alcuni autori hanno suggerito che la spagnola causò di fatto un effetto positivo per il guadagno pro-capite, nonostante la grande riduzione della forza lavoro e i gravi effetti di recessione a breve termine[49]. Altri studi hanno cercato di prevedere i costi di una pandemia grave come quella di influenza spagnola nell'economia statunitense, nel caso ipotizzato di un'infezione del 30% dei lavoratori, il 2,5% dei decessi e un periodo di malattia di tre settimane. Una tale situazione diminuirebbe il prodotto interno lordo del 5%. Ulteriori costi deriverebbero dal trattamento medico di un numero variabile da 18 a 45 milioni di persone e il costo totale si aggirerebbe attorno ai 700 miliardi di dollari[50].
Anche i costi per la prevenzione sono alti. I governi di tutto il mondo hanno speso miliardi di dollari per la preparazione e la pianificazione di una potenziale pandemia di influenza aviaria, i cui costi derivano dall'acquisto di farmaci e vaccini, oltre alla gestione dell'emergenza e le strategia per il controllo delle frontiere[51]. Il 1º novembre 2005 il presidente George W. Bush illustrò la strategia nazionale per la sicurezza contro l'influenza aviaria[52] e richiese al congresso 7,1 miliardi di dollari per l'implementazione del piano[53].
Nel 2006, più di 10 miliardi di dollari sono stati spesi e più di 200 milioni di volatili sono stati abbattuti per tentare di contenere l'influenza aviaria[54], tuttavia questi sforzi sono stati poco efficaci per il controllo della propagazione del virus, e ne sono stati tentati altri: ad esempio il governo vietnamita adottò una strategia combinata di vaccinazione del pollame di massa, disinfezione, abbattimento controllato, campagne di informazione e bando di pollame nelle città[55]. Come risultato il costo di allevamento aumentò, mentre il costo ai consumatori scese a causa del crollo della domanda.
Questo provocò perdite disastrose negli allevatori. Alcuni non riuscirono a mettere in pratica le misure che richiedevano di isolare l'allevamento dal contatto con volatili selvatici, rischiando di perdere l'allevamento. L'allevamento globale di pollame divenne poco redditizio all'aumentare dell'endemicità del virus nei volatili selvatici[56]. La rovina economica per alcuni allevatori provocò anche casi di suicidio, mentre altri non cooperarono con gli sforzi per contenere il virus[57][58].
Sorveglianza virologica ed epidemiologica in Italia[modifica | modifica wikitesto]
L'OMS svolge da cinquant'anni una sorveglianza continua e globale attraverso il Sistema globale di sorveglianza e di risposta all'influenza (Gisrs) a cui partecipano 110 Paesi. In Italia il (NIC-Centro Nazionale Influenza) opera all'interno del Dipartimento Malattie Infettive dell'Istituto Superiore di Sanità. Il NIC fa capo ad una rete di 14 laboratori, dislocati prevalentemente all'interno di strutture universitarie e distribuiti su tutto il territorio nazionale. I dati delle indagini di laboratorio sui ceppi circolanti durante la stagione influenzale forniscono indicazioni sulle variazioni antigeniche del virus e di conseguenza sulla formulazione dei vaccini.
All'interno di ogni Paese esiste poi, accanto alla sorveglianza virologica, anche un sistema di sorveglianza clinica. In Italia la sorveglianza clinico-epidemiologica viene svolta da una rete di circa 1000 medici di famiglia e pediatri "sentinella" che effettuano un monitoraggio sull'1.5% della popolazione nazionale.
Il periodo di sorveglianza epidemiologica è compreso tra la 42a settimana di ogni anno e la 17a dell'anno successivo, mentre il periodo di sorveglianza virologica tra la 46a settimana di ogni anno e la 17a dell'anno successivo. I risultati epidemiologici e virologici sono pubblicati settimanalmente sul sito del Ministero della Salute e sul sito dell'ISS.
C'è anche il progetto Influweb che utilizza l'attività di volontari-utenti web per il monitoraggio dell'influenza in Italia.
Eziologia[modifica | modifica wikitesto]

Alla famiglia Orthomyxoviridae appartengono tre tipi di virus influenzali: Influenzavirus A, Influenzavirus B e Influenzavirus C. Influenza A e C infettano diverse specie, mentre l'Influenza B quasi esclusivamente infetta l'uomo[59].
I virus A e B presentano in superficie 2 glicoproteine:
- Emoagglutinina (contrassegnata con la lettera H)
- Neuraminidasi (contrassegnata con la lettera N)
Influenzavirus A[modifica | modifica wikitesto]
I virus del tipo A sono i patogeni più virulenti nell'uomo e causano le malattie più gravi.
A seconda delle glicoproteine di superficie, il virus A si suddivide in sottotipi (o serotipi). Si conoscono 18 sottotipi di emoagglutinina (da H1 a H18) e 11 sottotipi di neuraminidasi (da N1 a N11)[60]. Tutti i sottotipi sono stati ritrovati nelle specie aviarie, mentre l'uomo e altri animali ospitano solo alcuni sottotipi: ciò significa che sono gli uccelli i serbatoi naturali del virus A. In particolare i volatili acquatici selvatici sono ospiti naturali per una grande varietà di virus di tipo A, che occasionalmente sono trasmessi alle altre specie e potrebbero essere la causa di focolai devastanti nel pollame domestico oppure di pandemie nell'uomo[61].
Le pandemie del 1918-19 (spagnola, causata dal sottotipo H1N1), 1957-58 (asiatica, causata dal sottotipo H2N2) e 1968-69 (Hong Kong, sottotipo H3N2) sono state effetto di un rimescolamento genico di virus aviari e umani, ma la trasmissione di un virus aviario all'uomo può causare una malattia grave anche senza rimescolamento (ad es. il focolaio avvenuto nel 1997 a Hong Kong a causa del virus A/H5N1). Fortunatamente questo sottotipo non riuscì a rimescolarsi e ad acquisire la capacità di trasmettersi da uomo a uomo.
Altri sottotipi la cui presenza è stata confermata nell'uomo sono:
- H7N7: Influenza con insolito potenziale zoonotico[62]
- H1N2: Influenza endemica nell'uomo e nei suini
- H9N2, H7N2, H7N3, H10N7.
Influenzavirus B[modifica | modifica wikitesto]
Il virus dell'Influenza B è quasi esclusivamente un patogeno umano ed è meno comune dell'influenza A. I soli animali conosciuti ad essere vulnerabili al virus B oltre all'uomo, sono i pinnipedi[63]. Questo tipo di influenza muta 2–3 volte meno rapidamente del tipo A[64] e di conseguenza ha una minore diversità genetica, con un solo serotipo[59]. A causa di questa scarsa diversità antigenica, normalmente si acquisisce un certo grado di immunità all'influenza B. Tuttavia, l'influenza B muta abbastanza velocemente per impedire una immunità permanente[65]. Il ridotto tasso di mutazione antigenica, combinata con una scarsa gamma di ospiti (che impedisce uno spostamento antigenico tra specie diverse) assicura l'impossibilità di pandemie di influenza B[66].
Influenzavirus C[modifica | modifica wikitesto]
L'influenza C infetta l'uomo e i suini e può causare gravi malattie ed epidemie locali[67]. Tuttavia, l'influenza C è meno comune rispetto agli altri tipi e normalmente sembra causare solo disturbi non troppo gravi nei bambini[68][69].
Deriva antigenica[modifica | modifica wikitesto]
I nuovi virus influenzali sono prodotti costantemente da mutazioni o da riassortimento. I piccoli cambiamenti negli antigeni emagglutinina e neuramidasi sulla superficie del virus sono mutazioni antigeniche minori. Questo fenomeno viene chiamato deriva antigenica (drift) e crea una "variante di ceppo". Uno di questi ceppi può infine raggiungere una maggiore virulenza, diventa dominante e si diffonde rapidamente nella popolazione, spesso causando un'epidemia[70].
Spostamento ("shift") antigenico[modifica | modifica wikitesto]
Quando il virus acquisisce antigeni del tutto nuovi, ad esempio per riassortimento tra i ceppi aviari e i ceppi umani, si parla invece di spostamento antigenico (antigenic shift). Se un virus di influenza umana viene prodotto con antigeni completamente nuovi, chiunque sarà vulnerabile e questo nuovo tipo di influenza può propagarsi senza controllo, causando una pandemia[71]. È stato proposto un modello alternativo, dove le pandemie periodiche sono prodotte dall'interazione di un insieme fisso di ceppi virali con una popolazione umana con un insieme di immunità in cambiamento continuo verso diverso ceppi virali[72].
Protezione incrociata[modifica | modifica wikitesto]
La protezione incrociata è il meccanismo che regola l'interazione fra una specifica variante genetica dell'influenza ed il sistema immunitario. Il sistema immunitario è in grado di contrastare tutte le varianti genetiche antigenicamente simili a quelle che in passato hanno infettato l'organismo.
La diversità antigenica fra varianti del virus non risulta proporzionale alla loro diversità genetica, cioè al numero di nucleotidi dissimili fra le sequenze nucleotidiche che codificano i loro antigeni. Infatti, mentre le mutazioni nelle sequenze nucleotidiche si manifestano in modo casuale e regolare nel tempo, l'evoluzione antigenica risulta molto irregolare.
In particolare nel tempo si osserva una successione di clusters di ceppi tra di loro molto simili e dissimili da quelli contenuti negli altri clusters. Quando un cluster si estingue, ne emerge uno nuovo che prende il suo posto.
Clinica[modifica | modifica wikitesto]
Si suole intendere con la parola influenza una malattia banale, blanda, in attrito con la storia di questa malattia che, in genere per complicanze batteriche, in passato ha falcidiato migliaia di vittime. Nell'era antibiotica le sovrainfezioni batteriche frequenti un tempo sono state scongiurate, ma la malattia mantiene le sue caratteristiche morbose.
Segni e sintomi[modifica | modifica wikitesto]
Tutti i sintomi dell'influenza sono comuni a molte altre malattie, il che porta a confonderla soprattutto con la faringite, la tonsillite e il raffreddore comune. È il quadro d'insieme ad aumentare l'attendibilità della diagnosi:
- Comparsa dei primi sintomi generalmente brusca e improvvisa, accompagnata da brividi e sudorazione.
- Febbre superiore ai 38°, di durata tra i 3 e i 4 giorni.
- Mal di testa.
- Malessere e dolori osteomuscolari, spesso forti.
- Affaticamento e debolezza, che, contrariamente alla febbre, possono durare fino a 2-3 settimane.
- Naso chiuso, a volte.
- Starnuti, a volte.
- Mal di gola, a volte.
- Comuni i dolori al petto durante la respirazione e soprattutto la tosse.
- Riduzione dell'appetito.
- Fotofobia.
- Aumentata suscettibilità di sviluppo di altre forme morbose (bronchiti, polmoniti).
- Spesso ci sono anche disturbi gastrointestinali, come nausea, diarrea e crampi addominali.
L'influenza può anche avere esito letale, specialmente in soggetti deboli, neonati, anziani o con malattie croniche[22].
Complicanze[modifica | modifica wikitesto]
La maggior parte delle persone che contrae l'influenza recupera in una o due settimane, ma gli individui più fragili possono sviluppare complicazioni pericolose come la polmonite. In base all'OMS: "Ogni inverno, decine di milioni di persone contraggono l'influenza. La maggior parte rimane a casa per circa una settimana. Altri, la maggior parte anziani, muoiono. Sappiamo che il conteggio dei morti a livello mondiale supera il centinaio di migliaia di persone l'anno, ma anche nelle nazioni sviluppate i numeri non sono sicuri, perché le autorità mediche normalmente non verificano i veri decessi per influenza e i decessi per malattie simili"[73].
Anche le persone in salute possono essere contagiate e conseguenze più gravi possono comparire ad ogni età. Le persone che hanno superato i 50 anni, i bambini molto piccoli e le persone di ogni età con patologie croniche sono più esposte alle complicazioni dell'influenza come polmoniti, bronchiti, sinusiti e infezioni alle orecchie.[74].
Inoltre l'influenza può peggiorare problemi di salute cronici già presenti. Le persone con enfisemi, bronchiti croniche o asma possono accusare insufficienza respiratoria mentre hanno l'influenza, mentre chi è affetto da coronaropatie o insufficienza cardiaca può sviluppare uno scompenso cardiaco acuto[75]. Anche il fumo costituisce un fattore di rischio associato con patologie più gravi e può incrementare la letalità dell'influenza[76].
Esami di laboratorio e strumentali[modifica | modifica wikitesto]
I test di laboratorio disponibili sono in continuo miglioramento. Il Center for Disease Control and Prevention statunitense conserva un elenco aggiornato dei test per l'influenza disponibili[77]. I test di diagnosi rapida hanno una sensibilità del 70-75%, e una specificità del 90-95% quando sono comparati con la coltura virale. Questi test possono essere particolarmente utili durante la stagione influenzale (prevalenza 25%) in assenza di un focolaio locale o stagione para-influenzale (prevalenza = 10%[78]).
La diagnosi può essere effettuata
- con l'isolamento del virus in colture cellulari di tamponi naso-faringei
- mediante titolazione di anticorpi specifici presenti nel siero dei pazienti
- con tecniche di biologia molecolare quali polymerase chain reaction (PCR) e RT-PCR in grado di distinguere l'RNA del virus influenzale da quello dei virus respiratori sinciziali o dei virus parainfluenzali umani.
Sono disponibili test rapidi eseguibili in ambulatorio, ma hanno una sensibilità e una specificità non superiore alla diagnosi clinica, pertanto possono essere d'aiuto solo nelle fasi iniziali o finali dell'epidemia. In corso di epidemia si tratta di procedure costose e del resto inutili. Gli studi di analisi decisionale[78][79] suggeriscono infatti che durante i focolai locali di influenza, la prevalenza è oltre il 70%[78], quindi i pazienti con qualunque combinazione di sintomi tra quelli sopra descritti può essere trattata con inibitori della neuraminidasi senza effettuare test. Anche in assenza di focolai locali, il trattamento può essere giustificato negli anziani durante la stagione influenzale quando la prevalenza supera il 15%[78]. Siccome i farmaci anti-virali nel trattamento dell'influenza sono tanto meno efficaci quanto meno tempestivamente somministrati, è importante iniziare il trattamento appena si ha una ragionevole certezza della malattia combinando gli elementi clinici con i dati epidemiologici locali.
Trattamento[modifica | modifica wikitesto]
I consigli generali sono il riposo, l'assunzione di liquidi, l'astinenza da bevande alcoliche e dal fumo. I bambini e gli adolescenti con sintomi influenzali (in particolare la febbre) non dovrebbero assumere acido acetilsalicilico (Aspirina) durante l'infezione (specialmente con il tipo B), perché potrebbe causare la sindrome di Reye, una patologia del fegato[80] rara, ma fatale. Siccome l'influenza è causata da un virus, gli antibiotici non hanno effetto sull'infezione; a meno di non essere stati prescritti per la prevenzione delle infezioni secondarie, come la polmonite batterica. I farmaci antivirali sono a volte efficaci, ma i virus possono sviluppare resistenze ai farmaci antivirali standard.
Le due classi di antivirali utilizzati sono gli inibitori della neuraminidasi e gli inibitori M2. I primi sono preferiti nelle infezioni da virus influenzali, mentre gli inibitori M2 sono stati raccomandati dal CDC durante la stagione influenzale 2005-2006[81]
Inibitori della neuraminidasi[modifica | modifica wikitesto]
I farmaci inibitori della neuraminidasi come l'oseltamivir (nome commerciale Tamiflu) e lo zanamivir (nome commerciale Relenza) sono stati progettati per bloccare la replicazione del virus nell'organismo[82]. Questi farmaci sono spesso efficaci contro l'influenza A e B[83] riducendone i sintomi e le complicanze.[84]. Altri ceppi di influenza possono presentare vari gradi di resistenza contro questi antivirali ed è impossibile prevedere quale grado di resistenza possono presentare in ceppi pandemici futuri[85].
Inibitori M2[modifica | modifica wikitesto]
I farmaci antivirali amantadina e rimantadina sono progettati per bloccare il canale ionico virale e prevenire l'infezione delle cellule da parte del virus. Questi farmaci sono a volte efficaci contro l'influenza A se sono stati somministrati in tempo, ma sono sempre inefficaci contro l'influenza B[83]. La resistenza all'amantadina e alla rimantadina in America dell'H3N2 è incrementata al 91% nel 2005[86].
Prevenzione[modifica | modifica wikitesto]
La prevenzione può essere maggiormente efficace se si osservano norme igieniche di base. Le persone che contraggono l'influenza sono maggiormente contagiose tra il secondo e il terzo giorno dopo l'infezione, e l'infettività dura per circa 10 giorni[87]. Generalmente i bambini sono più contagiosi degli adulti.[87][88]. La diffusa credenza che l'influenza sia collegata all'esposizione a temperature rigide, è ovviamente sbagliata e priva di fondamento scientifico.
La propagazione del virus avviene attraverso le particelle di aerosol e il contatto con superfici contaminate, quindi è importante persuadere le persone a coprirsi la bocca quando starnutiscono e lavarsi regolarmente le mani[89]. Nelle aree dove il virus può essere presente sulle superfici può essere raccomandabile la disinfezione delle stesse[90]. L'alcool è un agente disinfettante efficace, mentre l'uso di sali di ammonio quaternario può essere combinata con l'alcool per incrementare la durata dell'azione disinfettante[91]. Negli ospedali i disinfettanti a base di ammonio quaternario e agenti a rilascio di alogeni come l'ipoclorito di sodio sono utilizzati per la disinfezione delle stanze o degli arredi che sono stati utilizzati dai pazienti con sintomi influenzali. Durante le pandemie passate, la chiusura di scuole, chiese e teatri rallentò la diffusione del virus ma non ebbe un effetto significativo nel numero totale dei decessi[92][93].
Vaccinazione[modifica | modifica wikitesto]

I vaccini influenzali possono essere prodotti in vari modi; il metodo tradizionale consiste nel far crescere il virus in embrioni di pollo. Dopo la purificazione, il virus è inattivato (ad esempio, attraverso trattamenti con detergenti) per produrre un vaccino con un virus inattivato. In alternativa, il virus può essere coltivato in uova fino a quando perde la sua virulenza, in modo da produrre un vaccino vivo attenuato[22].
I vaccini costituiti da virus intero possono provocare la reazione del sistema immunitario come se il corpo fosse effettivamente infettato e possono apparire i sintomi dell'infezione (molti sintomi di influenza e raffreddore sono solo sintomi di infezione generale), anche se non sono gravi o durevoli come quelli provocati dalla vera infezione. Il più pericoloso effetto collaterale è costituito dalla reazione allergica sia al materiale virale che ai residui delle uova di gallina utilizzati per la coltura del virus. Queste reazioni tuttavia sono estremamente rare[94]. Il vaccino non deve essere somministrato a: bambini di età inferiore a 6 mesi; persone allergiche alle proteine dell'uovo (perché nella produzione industriale i virus influenzali vengono fatti crescere nelle uova di gallina).
Oltre che vaccini costituiti da virus intero attenuato o inattivato, oggi disponiamo di vaccini split, costituiti da particelle virali sottoposte a lisi, o di vaccini subunità (che contengono solo le glicoproteine che costituiscono il rivestimento esterno del virus). L'introduzione dei vaccini split e subunità ha permesso di azzerare gli effetti collaterali del vaccino.
L'efficacia dei vaccini è variabile. A causa delle rapide mutazioni del virus, un particolare vaccino solitamente conferisce protezione per un periodo non superiore al paio di anni. Ogni anno, l'OMS ricerca i ceppi che saranno in circolazione durante l'anno successivo, permettendo alle aziende farmaceutiche di sviluppare vaccini che forniscano la migliore immunità contro questi ceppi e possano essere utilizzati per la prevenzione o combinati con la soppressione di animali infetti per sradicare i focolai[95].
È tuttavia possibile essere vaccinati e contrarre l'influenza. Il vaccino viene riformulato ogni anno per alcuni ceppi specifici, ma non è possibile includere tutti i ceppi che infettano le persone nel mondo durante la stagione influenzale. La formulazione e la produzione delle milioni di dosi necessarie per l'epidemia stagionale richiede circa sei mesi; occasionalmente un ceppo nuovo o conosciuto diventa predominante durante questo periodo e infetta le persone, anche se sono state vaccinate (come nella stagione influenzale 2003-2004 con il ceppo H3N2)[96]. Inoltre è possibile essere infettati appena prima della vaccinazione e ammalarsi con il ceppo che dovrebbe essere prevenuto dal vaccino, poiché quest'ultimo impiega circa due settimane per diventare efficace[74].
Soggetti a cui è raccomandata la vaccinazione[modifica | modifica wikitesto]
La vaccinazione contro il virus è fortemente raccomandata per i soggetti ad alto rischio come anziani, diabetici, cardiopatici, pazienti con malattie respiratorie, neoplastiche o con deficit immunitari.
Nella stagione 2006-2007, per la prima volta il CDC ha raccomandato la vaccinazione dei bambini con età inferiore a 59 mesi[89].
La vaccinazione ha comunque un elevato valore sociale, dati i costi che il contagio e la malattia comportano: vaccinarsi per l'influenza, quindi, comporterebbe anche dei vantaggi sul piano della spesa sanitaria.
Infezione negli animali[modifica | modifica wikitesto]
L'influenza infetta molte specie di animali e può avvenire il trasferimento di ceppi virali tra specie diverse. I volatili sono considerati i principali ospiti di virus influenzali[97]. Tutti i sottotipi noti (identificati con la sigla HxNy) sono stati trovati nei volatili ma molti sottotipi sono endemici nell'uomo, nel cane, nel cavallo e nei suini; segni di infezioni sono state trovate anche in gatti, pinnipedi, cammelli, furetti e balene[65]. Le varianti del virus influenzale sono a volte chiamate in accordo con la specie in cui quel particolare ceppo è endemico. Le varianti principali sono quindi: Influenza aviaria, Influenza umana, Influenza equina, Influenza canina, Influenza suina (l'Influenza felina si riferisce generalmente alla Rinotracheite virale felina o Calicivirus felino e non l'infezione da un virus influenzale). Nei maiali, nei cavalli e nei cani i sintomi sono simili a quelli che compaiono nell'uomo, con febbre, tosse e perdita di appetito[65]. La frequenza negli animali non è stata studiata accuratamente come nell'uomo, tuttavia ad esempio i focolai di infezione nei suini sono comuni e non sono mortali[65].
I sintomi nei volatili sono variabili e possono essere aspecifici[98]. I sintomi che seguono le infezioni con bassa patogenicità possono essere piumaggio increspato, riduzione della produzione di uova o perdita di peso combinata con disturbi respiratori[99]. Queste sintomi rendono le diagnosi sul campo difficili, poiché il tracciamento di una epidemia richiede test di laboratorio di campioni prelevati da esemplari infetti. Alcuni ceppi come l'H9N2 sono altamente virulenti nel pollame e possono causare sintomi gravi e tassi di letalità significativi[100]. Nella sua forma più patogenica, l'influenza dei polli e dei tacchini produce una veloce comparsa di sintomi gravi che comportano il decesso in quasi il 100% dei casi entro due giorni[101]. Man mano che il virus si propaga in allevamenti intensivi di polli, questi focolai possono procurare grandi perdite economiche agli allevatori.
Un ceppo di H5N1 (chiamato HPAI A(H5N1), "virus di influenza aviaria altamente patogenico di tipo A e sottotipo H5N1"), altamente patogenico ed adattato da quello aviario provoca l'influenza H5N1, chiamata comunemente influenza aviaria, ed è endemica in molte popolazioni di volatili, specialmente nel sudest asiatico. Questo ceppo asiatico si è diffuso a livello globale. È epizootico (epidemico negli animali, tranne l'uomo) e panzootico (una malattia che colpisce gli animali di molte specie, specialmente su una grande area) e ha ucciso decine di milioni di volatili, comportando l'abbattimento di centinaia di milioni di altri volatili per controllare il propagarsi del virus[102][103].
Attualmente l'HPAI A(H5N1) è una malattia aviaria e non ci sono prove che suggeriscono una trasmissione efficiente da uomo a uomo del virus. In quasi tutti i casi le persone infettate hanno avuto contatti fisici con volatili infetti[104]. Nel futuro, l'H5N1 potrebbe mutare o subire un riassortimento in un nuovo ceppo in grado di trasmettersi efficacemente da uomo a uomo. A causa dell'elevata letalità, virulenza, presenza endemica e vasta gamma di ospiti, il virus H5N1 è la minaccia pandemica maggiore nel mondo, e di conseguenza sono stati e saranno spesi ingenti quantitativi di risorse per la preparazione ad una pandemia potenziale[51].
Note[modifica | modifica wikitesto]
- ^ Influenza (Seasonal), su who.int, World Health Organization. URL consultato il 19 dicembre 2015 (archiviato il 21 aprile 2018).
- ^ Patrick R. Murray, Ken Rosenthal e Michael Pfaller, Microbiologia medica, Questa traduzione del volume Medical Microbiogy è pubblicata in accordo con Elsevier Inc., Milano, Edra, ISBN 88-214-4377-9. URL consultato il 6 marzo 2018 (archiviato il 6 marzo 2018).«Il termine influenza, tuttavia, viene erroneamente usato anche per altre influenze respiratorie e virali (ad esempio, "influenza intestinale").»
- ^ Harrison's, cap. 187.
- ^ G. Brankston, L. Gitterman; Z. Hirji; C. Lemieux; M. Gardam, Transmission of influenza A in human beings., in Lancet Infect Dis, vol. 7, n. 4, Apr 2007, pp. 257-65, DOI:10.1016/S1473-3099(07)70029-4, PMID 17376383.
- ^ Centers of Disease Control and Prevention, USA.gov: Key Facts about Influenza (Flu) & Flu Vaccine, su cdc.gov. URL consultato il 19 dicembre 2015 (archiviato dall'url originale il 28 aprile 2019).
- ^ T. Jefferson, CB. Del Mar; L. Dooley; E. Ferroni; LA. Al-Ansary; GA. Bawazeer; ML. van Driel; S. Nair; MA. Jones; S. Thorning; JM. Conly, Physical interventions to interrupt or reduce the spread of respiratory viruses., in Cochrane Database Syst Rev, n. 7, 2011, pp. CD006207, DOI:10.1002/14651858.CD006207.pub4, PMID 21735402.
- ^ B. Michiels, K. Van Puyenbroeck; V. Verhoeven; E. Vermeire; S. Coenen, The value of neuraminidase inhibitors for the prevention and treatment of seasonal influenza: a systematic review of systematic reviews., in PLoS One, vol. 8, n. 4, 2013, pp. e60348, DOI:10.1371/journal.pone.0060348, PMID 23565231.
- ^ MH. Ebell, M. Call; J. Shinholser, Effectiveness of oseltamivir in adults: a meta-analysis of published and unpublished clinical trials., in Fam Pract, vol. 30, n. 2, Apr 2013, pp. 125-33, DOI:10.1093/fampra/cms059, PMID 22997224.
- ^ Copia archiviata, su who.int. URL consultato il 18 dicembre 2015 (archiviato il 22 ottobre 2009).
- ^ S.R. Palmer, Oxford Textbook of Zoonoses: Biology, Clinical Practice, and Public Health Control, OUP Oxford, 2011, p. 332, ISBN 978-0-19-857002-8.
- ^ P Martin, Martin-Granel E, 2,500-year evolution of the term epidemic, in Emerg Infect Dis, vol. 12, n. 6, giugno 2006, PMID 16707055. URL consultato il 26 gennaio 2008 (archiviato dall'url originale il 30 aprile 2011).
- ^ Hippocrates, Adams, Francis (transl.), Of the Epidemics, su classics.mit.edu, 400 BCE. URL consultato il 18 ottobre 2006 (archiviato dall'url originale il 5 ottobre 2006).
- ^ a b c "L'epidemiologia dell'influenza", Martin M.Kaplan e Robert G.Webster, pubbl. su "Le Scienze (Scientific American)", num.114, febbr.1978, pag.84-94
- ^ a b c CW Potter, A History of Influenza, in J Appl Microbiol., vol. 91, n. 4, ottobre 2006, pp. 572–579, DOI:10.1046/j.1365-2672.2001.01492.x, PMID 11576290.
- ^ a b c J Taubenberger, Morens D, 1918 Influenza: the mother of all pandemics., in Emerg Infect Dis, vol. 12, n. 1, 2006, pp. 15–22, PMID 16494711. URL consultato il 26 gennaio 2008 (archiviato dall'url originale il 3 settembre 2011).
- ^ a b KD Patterson, Pyle GF, The geography and mortality of the 1918 influenza pandemic., in Bull Hist Med., vol. 65, n. 1, Spring 1991, pp. 4–21, PMID 2021692.
- ^ a b c d e Knobler S, Mack A, Mahmoud A, Lemon S (a cura di), 1: The Story of Influenza, in The Threat of Pandemic Influenza: Are We Ready? Workshop Summary (2005)[collegamento interrotto], Washington, D.C., National Academies Press, pp. 60–61.
- ^ J Taubenberger, Reid A, Janczewski T, Fanning T, Integrating historical, clinical and molecular genetic data in order to explain the origin and virulence of the 1918 Spanish influenza virus. [collegamento interrotto], in Philos Trans R Soc Lond B Biol Sci, vol. 356, n. 1416, Dec 29 2001, pp. 1829–39, PMID 11779381.
- ^ L Simonsen, Clarke M, Schonberger L, Arden N, Cox N, Fukuda K, Pandemic versus epidemic influenza mortality: a pattern of changing age distribution., in J Infect Dis, vol. 178, n. 1, luglio 1998, pp. 53–60, PMID 9652423.
- ^ Michaelis M, Doerr HW, Cinatl J, Novel swine-origin influenza A virus in humans: another pandemic knocking at the door, in Medical Microbiology and Immunology, vol. 198, n. 3, agosto 2009, pp. 175–83, DOI:10.1007/s00430-009-0118-5, PMID 19543913.
- ^ Petrovski BÉ, Lumi X, Znaor L, Ivastinović D, Confalonieri F, Petrovič MG, Petrovski G, Reorganize and survive-a recommendation for healthcare services affected by COVID-19-the ophthalmology experience, in Eye, vol. 34, n. 7, luglio 2020, pp. 1177–1179, DOI:10.1038/s41433-020-0871-7, PMC 7169374, PMID 32313170.
- ^ a b c d M Hilleman, Realities and enigmas of human viral influenza: pathogenesis, epidemiology and control., in Vaccine, vol. 20, 25–26, Aug 19 2002, pp. 3068–87, PMID 12163258.
- ^ Centers for Disease Control and Prevention. Interim Pre-pandemic Planning Guidance: Community Strategy for Pandemic Influenza Mitigation in the United States Archiviato il 27 agosto 2009 in Internet Archive., February 2007 (pag.32)
- ^ a b Pandemic Influenza Risk Management: WHO Interim Guidance, su Organizzazione mondiale della sanità, 2013, p. 19 (archiviato dall'url originale il 21 gennaio 2021).
- ^ K Shimizu, History of influenza epidemics and discovery of influenza virus, in Nippon Rinsho, vol. 55, n. 10, ottobre 1997, pp. 2505–201, PMID 9360364.
- ^ W Smith, Andrewes CH, Laidlaw PP, A virus obtained from influenza patients, in Lancet, vol. 2, 1933, pp. 66–68.
- ^ Sir Frank Macfarlane Burnet: Biography Archiviato il 5 ottobre 2017 in Internet Archive. The Nobel Foundation. Accessed 22 Oct 06
- ^ H Kendall, Vaccine Innovation: Lessons from World War II [collegamento interrotto], in Journal of Public Health Policy, vol. 27, n. 1, 2006, pp. 38–57.
- ^ Influenza A Virus Genome Project Archiviato il 22 maggio 2006 in Archive.is. at The Institute of Genomic Research. Accessed 19 Oct 06
- ^ Subbarao K, Katz J, Influenza vaccines generated by reverse genetics., in Curr Top Microbiol Immunol, vol. 283, pp. 313-42, PMID 15298174.
- ^ Bardiya N, Bae J, Influenza vaccines: recent advances in production technologies., in Appl Microbiol Biotechnol, vol. 67, n. 3, 2005, pp. 299–305, PMID 15660212. URL consultato il 26 gennaio 2008 (archiviato dall'url originale il 26 marzo 2020).
- ^ Neirynck S, Deroo T, Saelens X, Vanlandschoot P, Jou WM, Fiers W, A universal influenza A vaccine based on the extracellular domain of the M2 protein, Nat Med. 1999 Oct;5(10):1157-63
- ^ Fiers W, Neirynck S, Deroo T, Saelens X, Jou WM, Soluble recombinant influenza vaccines, Philos Trans R Soc Lond B Biol Sci. 2001 Dec 29;356(1416):1961-3
- ^ Fiers W, De Filette M, Birkett A, Neirynck S, Min Jou W, A universal human influenza A vaccine, Virus Res. 2004 Jul;103(1-2):173-6
- ^ Recommended composition of influenza virus vaccines for use in the 2006–2007 influenza season Archiviato il 28 maggio 2006 in Internet Archive. WHO report 2006-02-14. Accessed 19 October 2006
- ^ Weather and the Flu Season Archiviato il 24 giugno 2017 in Internet Archive. NPR Day to Day, December 17 2003. Accessed, 19 October 2006
- ^ Lowen AC, Mubareka S, Steel J, Palese P, Influenza virus transmission is dependent on relative humidity and temperature, in PLoS Pathog., vol. 3, n. 10, 2007, pp. 1470–6, PMID 17953482.
- ^ Shek LP, Lee BW. "Epidemiology and seasonality of respiratory tract virus infections in the tropics." Paediatr Respir Rev. 2003 Jun;4(2):105–11. PMID 12758047
- ^ Dushoff J, Plotkin JB, Levin SA, Earn DJ. "Dynamical resonance can account for seasonality of influenza epidemics." Proc Natl Acad Sci U S A. 30 novembre 2004;101(48):16915–6. PMID 15557003
- ^ WHO Confirmed Human Cases of H5N1 Archiviato il 18 febbraio 2004 in Internet Archive. Data published by WHO Epidemic and Pandemic Alert and Response (EPR). Accessed 24 Oct. 2006
- ^ J Cannell, Vieth R, Umhau J, Holick M, Grant W, Madronich S, Garland C, Giovannucci E, Epidemic influenza and vitamin D, in Epidemiol Infect, vol. 134, n. 6, 2006, pp. 1129–40, PMID 16959053.
- ^ R HOPE-SIMPSON, The nature of herpes zoster: a long-term study and a new hypothesis, in Proc R Soc Med, vol. 58, pp. 9–20, PMID 14267505.
- ^ L Linday, Shindledecker R, Tapia-Mendoza J, Dolitsky J, Effect of daily cod liver oil and a multivitamin-mineral supplement with selenium on upper respiratory tract pediatric visits by young, inner-city, Latino children: randomized pediatric sites, in Ann Otol Rhinol Laryngol, vol. 113, n. 11, 2004, pp. 891–901, PMID 15562899.
- ^ Influenza Archiviato il 21 aprile 2018 in Internet Archive. WHO Fact sheet No. 211 revised March 2003. Accessed 22 October 2006
- ^ W Thompson, Shay D, Weintraub E, Brammer L, Cox N, Anderson L, Fukuda K, Mortality associated with influenza and respiratory syncytial virus in the United States, in JAMA, vol. 289, n. 2, 2003, pp. 179–86, PMID 12517228. URL consultato il 26 gennaio 2008 (archiviato il 10 febbraio 2008).
- ^ W Thompson, Shay D, Weintraub E, Brammer L, Bridges C, Cox N, Fukuda K, Influenza-associated hospitalizations in the United States, in JAMA, vol. 292, n. 11, 2004, pp. 1333–40, PMID 15367555. URL consultato il 26 gennaio 2008 (archiviato il 29 ottobre 2007).
- ^ Flu factsheet Archiviato il 13 ottobre 2005 in Internet Archive. National Institute of Allergy and Infectious Diseases Accessed 22 Dec 2006
- ^ Statement from President George W. Bush on Influenza Archiviato il 9 gennaio 2009 in Internet Archive. Accessed 26 Oct 2006
- ^ Brainerd, E. and M. Siegler (2003), “The Economic Effects of the 1918 Influenza Epidemic”, CEPR Discussion Paper, no. 3791.
- ^ Poland G, Vaccines against avian influenza—a race against time., in N Engl J Med, vol. 354, n. 13, 2006, pp. 1411–3, PMID 16571885. URL consultato il 26 gennaio 2008 (archiviato il 30 dicembre 2007).
- ^ a b Rosenthal, E. and Bradsher, K. Is Business Ready for a Flu Pandemic? Archiviato il 13 gennaio 2016 in Internet Archive. The New York Times 16-03-2006 Accessed 17-04-2006
- ^ National Strategy for Pandemic Influenza Archiviato il 9 gennaio 2009 in Internet Archive. Whitehouse.gov Accessed 26 Oct 2006.
- ^ Bush Outlines $7 Billion Pandemic Flu Preparedness Plan Archiviato il 14 settembre 2006 in Internet Archive. State.gov. Accessed 26 Oct 2006
- ^ US AID, Avian Influenza and its Global Implications (PDF), su usaid.gov. URL consultato il 26 ottobre 2006 (archiviato dall'url originale il 15 agosto 2008).
- ^ Lye DC, Ang BS, Leo YS, Review of human infections with avian influenza H5N1 and proposed local clinical management guideline, in Ann. Acad. Med. Singap., vol. 36, n. 4, 2007, pp. 285–92, PMID 17483860.
- ^ Poultry sector suffers despite absence of bird flu Archiviato il 29 novembre 2006 in Internet Archive. UN Office for the Coordination of Humanitarian Affairs. Accessed 26 Oct 2006
- ^ Nine poultry farmers commit suicide in flu-hit India Archiviato l'8 giugno 2007 in Internet Archive. Reuters. Published on April 12, 2006. Accessed 26 Oct 2006.
- ^ In the Nile Delta, Bird Flu Preys on Ignorance and Poverty Archiviato il 16 dicembre 2018 in Internet Archive. The New York Times. Published on April 13, 2006. Accessed 26 Oct 2006.
- ^ a b A Hay, Gregory V, Douglas A, Lin Y, The evolution of human influenza viruses, in Philos Trans R Soc Lond B Biol Sci, vol. 356, n. 1416, Dec 29 2001, pp. 1861–70, PMID 11779385.
- ^ Ying Wu, Yan Wu, Boris Tefsen, Yi Shi, George F. Gao, Bat-derived influenza-like viruses H17N10 and H18N11, in Trends in Microbiology, vol. 22, n. 4, 2014, pp. 183-191, DOI:10.1016/j.tim.2014.01.010.
- ^ Klenk et al, Avian Influenza: Molecular Mechanisms of Pathogenesis and Host Range, in Animal Viruses: Molecular Biology, Caister Academic Press, 2008, ISBN 978-1-904455-22-6.
- ^ R Fouchier, Schneeberger P, Rozendaal F, Broekman J, Kemink S, Munster V, Kuiken T, Rimmelzwaan G, Schutten M, Van Doornum G, Koch G, Bosman A, Koopmans M, Osterhaus A, Avian influenza A virus (H7N7) associated with human conjunctivitis and a fatal case of acute respiratory distress syndrome., in Proc Natl Acad Sci U S A, vol. 101, n. 5, 2004, pp. 1356–61, PMID 14745020. URL consultato il 26 gennaio 2008 (archiviato il 12 gennaio 2008).
- ^ A Osterhaus, Rimmelzwaan G, Martina B, Bestebroer T, Fouchier R, Influenza B virus in seals., in Science, vol. 288, n. 5468, 2000, pp. 1051–3, PMID 10807575.
- ^ E Nobusawa, Sato K, Comparison of the mutation rates of human influenza A and B viruses, in J Virol, vol. 80, n. 7, aprile 2006, pp. 3675–8, PMID 16537638.
- ^ a b c d Webster R, Bean W, Gorman O, Chambers T, Kawaoka Y, Evolution and ecology of influenza A viruses., in Microbiol Rev, vol. 56, n. 1, 1992, pp. 152–79, PMID 1579108.
- ^ M Zambon, Epidemiology and pathogenesis of influenza., in J Antimicrob Chemother, 44 Suppl B, novembre 1999, pp. 3–9, PMID 10877456. URL consultato il 2 maggio 2019 (archiviato dall'url originale il 1º luglio 2009).
- ^ Y Matsuzaki, Sugawara K, Mizuta K, Tsuchiya E, Muraki Y, Hongo S, Suzuki H, Nakamura K, Antigenic and genetic characterization of influenza C viruses which caused two outbreaks in Yamagata City, Japan, in 1996 and 1998, in J Clin Microbiol, vol. 40, n. 2, 2002, pp. 422–9, PMID 11825952.
- ^ Y Matsuzaki, Katsushima N, Nagai Y, Shoji M, Itagaki T, Sakamoto M, Kitaoka S, Mizuta K, Nishimura H, Clinical features of influenza C virus infection in children., in J Infect Dis, vol. 193, n. 9, 1º maggio 2006, pp. 1229–35, PMID 16586359.
- ^ S Katagiri, Ohizumi A, Homma M, An outbreak of type C influenza in a children's home., in J Infect Dis, vol. 148, n. 1, luglio 1983, pp. 51–6, PMID 6309999.
- ^ Long intervals of stasis punctuated by bursts of positive selection in the seasonal evolution of influenza A virus, in Biol Direct, vol. 1, n. 1, 2006, p. 34, PMID 17067369.
- ^ C Parrish, Kawaoka Y, The origins of new pandemic viruses: the acquisition of new host ranges by canine parvovirus and influenza A viruses, in Annual Rev Microbiol, vol. 59, pp. 553–86, PMID 16153179.
- ^ Recker M, Pybus OG, Nee S, Gupta S, The generation of influenza outbreaks by a network of host immune responses against a limited set of antigenic types, in Proc Natl Acad Sci U S A., vol. 104, n. 18, 2007, pp. 7711–7716, PMID 17460037. URL consultato il 26 gennaio 2008 (archiviato il 29 febbraio 2008).
- ^ Peter M. Sandman and Jody Lanard "Bird Flu: Communicating the Risk" Archiviato il 23 aprile 2011 in Internet Archive. 2005 Perspectives in Health Magazine Vol. 10 issue 2.
- ^ a b Key Facts about Influenza (Flu) Vaccine Archiviato il 28 febbraio 2018 in Internet Archive. CDC publication. Published October 17, 2006. Accessed 18 Oct 2006.
- ^ Angelo SJ, Marshall PS, Chrissoheris MP, Chaves AM. "Clinical characteristics associated with poor outcome in patients acutely infected with Influenza A." Conn Med. 2004 Apr;68(4):199–205. PMID 15095826
- ^ Murin S, Bilello K, Respiratory tract infections: another reason not to smoke., in Cleve Clin J Med, vol. 72, n. 10, 2005, pp. 916-20, PMID 16231688.
- ^ Centers for Disease Control and Prevention. Lab Diagnosis of Influenza. Archiviato il 31 dicembre 2007 in Internet Archive. Accessed on January 1, 2007
- ^ a b c d Rothberg M, Bellantonio S, Rose D, Management of influenza in adults older than 65 years of age: cost-effectiveness of rapid testing and antiviral therapy., in Ann Intern Med, vol. 139, 5 Pt 1, 2003, pp. 321-9, PMID 12965940. URL consultato il 26 gennaio 2008 (archiviato dall'url originale il 26 gennaio 2008).
- ^ Smith K, Roberts M, Cost-effectiveness of newer treatment strategies for influenza., in Am J Med, vol. 113, n. 4, 2002, pp. 300-7, DOI:10.1016/S0002-9343(02)01222-6, PMID 12361816.
- ^ J Glasgow, Middleton B, Reye syndrome — insights on causation and prognosis, in Arch Dis Child, vol. 85, n. 5, 2001, pp. 351–3, PMID 11668090. URL consultato il 26 gennaio 2008 (archiviato dall'url originale il 4 ottobre 2006).
- ^ Centers for Disease Control and Prevention. CDC Recommends against the Use of Amantadine and Rimantadine for the Treatment or Prophylaxis of Influenza in the United States during the 2005–06 Influenza Season. Archiviato il 3 maggio 2008 in Internet Archive. January 14, 2006. Retrieved on 2007-01-01
- ^ A Moscona, Neuraminidase inhibitors for influenza, in N Engl J Med, vol. 353, n. 13, 2005, pp. 1363–73, PMID 16192481. URL consultato il 26 gennaio 2008 (archiviato il 2 gennaio 2008).
- ^ a b I Stephenson, Nicholson K, Chemotherapeutic control of influenza, in J Antimicrob Chemother, vol. 44, n. 1, 1999, pp. 6–10, PMID 10459804. URL consultato il 2 maggio 2019 (archiviato il 23 gennaio 2009).
- ^ T Jefferson, Demicheli V, Di Pietrantonj C, Jones M, Rivetti D, Neuraminidase inhibitors for preventing and treating influenza in healthy adults, in Cochrane Database Syst Rev, vol. 3, pp. CD001265, DOI:10.1002/14651858.CD001265.pub2, PMID 16855962.
- ^ Robert G. Webster, H5N1 Influenza — Continuing Evolution and Spread, in N Engl J Med, vol. 355, n. 21, 2006, pp. 2174–77, PMID 16192481. URL consultato il 26 gennaio 2008 (archiviato il 5 dicembre 2006).
- ^ High levels of adamantane resistance among influenza A (H3N2) viruses and interim guidelines for use of antiviral agents — United States, 2005–06 influenza season, in MMWR Morb Mortal Wkly Rep, vol. 55, n. 2, 2006, pp. 44–6, PMID 16424859. URL consultato il 26 gennaio 2008 (archiviato il 6 gennaio 2008).
- ^ a b Carrat F, Luong J, Lao H, Sallé A, Lajaunie C, Wackernagel H, A 'small-world-like' model for comparing interventions aimed at preventing and controlling influenza pandemics, in BMC Med, vol. 4, p. 26, PMID 17059593.
- ^ Mitamura K, Sugaya N, [Diagnosis and Treatment of influenza—clinical investigation on viral shedding in children with influenza], in Uirusu, vol. 56, n. 1, 2006, pp. 109-16, PMID 17038819.
- ^ a b Prevention and Control of Influenza: Recommendations of the Advisory Committee on Immunization Practices (ACIP) Archiviato il 14 febbraio 2008 in Internet Archive. CDC report (MMWR 2006 Jul 28;55(RR10):1–42) accessed 19 Oct 2006.
- ^ Hota B, Contamination, disinfection, and cross-colonization: are hospital surfaces reservoirs for nosocomial infection?, in Clin Infect Dis, vol. 39, n. 8, 2004, pp. 1182–9, PMID 15486843.
- ^ McDonnell G, Russell A, Antiseptics and disinfectants: activity, action, and resistance, in Clin Microbiol Rev, vol. 12, n. 1, 1999, pp. 147-79, PMID 9880479. URL consultato il 26 gennaio 2008 (archiviato dall'url originale il 22 ottobre 2008).
- ^ Hatchett RJ, Mecher CE, Lipsitch M, Public health interventions and epidemic intensity during the 1918 influenza pandemic, in Proc Natl Acad Sci U S A., vol. 104, n. 18, 2007, pp. 7582–7587, PMID 17416679. URL consultato il 26 gennaio 2008 (archiviato il 9 marzo 2008).
- ^ Bootsma MC, Ferguson NM, The effect of public health measures on the 1918 influenza pandemic in U.S. cities, in Proc Natl Acad Sci U S A., vol. 104, n. 18, 2007, pp. 7588–7593, PMID 17416677. URL consultato il 26 gennaio 2008 (archiviato il 22 marzo 2020).
- ^ Questions & Answers: Flu Shot Archiviato il 17 luglio 2018 in Internet Archive. CDC publication updated Jul 24, 2006. Accessed 19 Oct 06.
- ^ I Capua, Alexander D, The challenge of avian influenza to the veterinary community., in Avian Pathol, vol. 35, n. 3, 2006, pp. 189–205, PMID 16753610. URL consultato il 26 gennaio 2008 (archiviato il 23 ottobre 2008).
- ^ E Holmes, Ghedin E, Miller N, Taylor J, Bao Y, St George K, Grenfell B, Salzberg S, Fraser C, Lipman D, Taubenberger J, Whole-genome analysis of human influenza A virus reveals multiple persistent lineages and reassortment among recent H3N2 viruses, in PLoS Biol, vol. 3, n. 9, 2005, pp. e300, PMID 16026181.
- ^ Gorman O, Bean W, Kawaoka Y, Webster R, Evolution of the nucleoprotein gene of influenza A virus., in J Virol, vol. 64, n. 4, 1990, pp. 1487–97, PMID 2319644.
- ^ Elbers A, Koch G, Bouma A, Performance of clinical signs in poultry for the detection of outbreaks during the avian influenza A (H7N7) epidemic in The Netherlands in 2003., in Avian Pathol, vol. 34, n. 3, 2005, pp. 181-7, PMID 16191700.
- ^ Capua I, Mutinelli F. "Low pathogenicity (LPAI) and highly pathogenic (HPAI) avian influenza in turkeys and chicken." In: Capua I, Mutinelli F. (eds.), A Colour Atlas and Text on Avian Influenza, Papi Editore, Bologna, 2001, pp. 13–20
- ^ Bano S, Naeem K, Malik S, Evaluation of pathogenic potential of avian influenza virus serotype H9N2 in chickens., in Avian Dis, vol. 47, 3 Suppl, 2003, pp. 817-22, PMID 14575070.
- ^ Swayne D, Suarez D, Highly pathogenic avian influenza., in Rev Sci Tech, vol. 19, n. 2, 2000, pp. 463-82, PMID 10935274.
- ^ Li K, Guan Y, Wang J, Smith G, Xu K, Duan L, Rahardjo A, Puthavathana P, Buranathai C, Nguyen T, Estoepangestie A, Chaisingh A, Auewarakul P, Long H, Hanh N, Webby R, Poon L, Chen H, Shortridge K, Yuen K, Webster R, Peiris J, Genesis of a highly pathogenic and potentially pandemic H5N1 influenza virus in eastern Asia., in Nature, vol. 430, n. 6996, 2004, pp. 209-13, PMID 15241415.
- ^ Li KS, Guan Y, Wang J, Smith GJ, Xu KM, Duan L, Rahardjo AP, Puthavathana P, Buranathai C, Nguyen TD, Estoepangestie AT, Chaisingh A, Auewarakul P, Long HT, Hanh NT, Webby RJ, Poon LL, Chen H, Shortridge KF, Yuen KY, Webster RG, Peiris JS. "The Threat of Pandemic Influenza: Are We Ready?" Workshop Summary Archiviato il 14 settembre 2006 in Internet Archive. National Academies Press (2005) "Today's Pandemic Threat: Genesis of a Highly Pathogenic and Potentially Pandemic H5N1 Influenza Virus in Eastern Asia", pages 116–130
- ^ Liu J, Avian influenza—a pandemic waiting to happen? (PDF), in J Microbiol Immunol Infect, vol. 39, n. 1, 2006, pp. 4–10, PMID 16440117 (archiviato dall'url originale il 16 febbraio 2008).
Bibliografia[modifica | modifica wikitesto]
- Dan L. Longo et al., Harrison's Principles of Internal Medicine, 18ª ed., The McGraw-Hill, 2012, ISBN 978-0-07-174889-6.
Altri progetti[modifica | modifica wikitesto]
 Wikiquote contiene citazioni sull'influenza
Wikiquote contiene citazioni sull'influenza Wikizionario contiene il lemma di dizionario «influenza»
Wikizionario contiene il lemma di dizionario «influenza» Wikimedia Commons contiene immagini o altri file sull'influenza
Wikimedia Commons contiene immagini o altri file sull'influenza
Collegamenti esterni[modifica | modifica wikitesto]
- (IT, DE, FR) Influenza, su hls-dhs-dss.ch, Dizionario storico della Svizzera.
- (EN) influenza, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Influenza (Istituto Superiore di Sanità - EpiCentro), su epicentro.iss.it.
- ECDC European Centre for Disease Prevention and Control.
| Controllo di autorità | Thesaurus BNCF 16187 · LCCN (EN) sh85066127 · GND (DE) 4022090-4 · BNF (FR) cb11949457x (data) · J9U (EN, HE) 987007550726005171 · NSK (HR) 000058166 · NDL (EN, JA) 00569893 |
|---|