Kemisk polaritet
 For alternative betydninger, se Polaritet.
For alternative betydninger, se Polaritet.
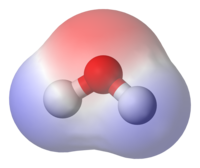
I kemi refererer polaritet til en ladningsforskydelse inden for et molekyle, hvormed én eller flere dele af molekylet bliver en anelse negativt og resten positivt. Denne polarisering skyldes forskel i elektronegativiteten mellem de forskellige komponenter af molekylet samt asymmetrien i strukturen.
Polære stoffer[redigér | rediger kildetekst]
Et polært stof er et stof der har en positivt elektrisk ladet ende (+pol) og en negativt elektrisk ladet ende.
At vand er polært skyldes forskellen i elektronegativitet mellem hydrogen og oxygen. Oxygen har en elektronegativitet på 3,44 mens hydrogen ligger på 2,2. Elektronskyen er således forskudt fra hydrogen over mod oxygen, hvilket gør hydrogenatomerne en smule positivt ladede i forhold til oxygen. Kombineret med at atomerne danner en vinkel, dannes der således en negativ pol i 'oxygenenden', mens der i den ende, hvor de to H-atomer sidder, dannes en positiv pol. Et sådant molekyle kaldes en dipol. Ladningerne markeres med lille delta minus (δ-) og lille delta plus (δ+), og upolære stoffer har en forskel i elektronegativitet på under en halv, mens polære stoffer har en forskel på mellem en halv og to.
Hydrogenatomernes vinkel på 104,45˚ skyldes at det er den vinkel, der kræver mindst energi at opretholde.
Vand kan blande sig med andre polære stoffer, fordi molekylernes negative pol tiltrækkes af en positiv pol ved det andet stof og omvendt.
Upolære stoffer[redigér | rediger kildetekst]
Et upolært stof er et stof der ikke indeholder grundstoffer med tilstrækkelig stor forskel i elektronegativitet til at danne en positivt elektrisk ladet ende og en negativt elektrisk ladet ende. Upolære stoffer kan desuden ikke danne hydrogenbindinger.
Eksempelvis er heptan (dvs. rensebenzin) et upolært stof der bruges som opløsningsmiddel for andre upolære stoffer som f.eks. fedtstof.
Et upolært stof er, modsat polære stoffer, et symmetrisk molekyle. Ladningsfordelingen er altså symmetrisk, og der opstår ikke poler i nogen ’ender’. Et upolært stof kunne f.eks. være det organiske opløsningsmiddel pentan, der består af 5 kulstofatomer/carbonatomer og 12 brintatomer/hydrogenatomer. Pentan er et alkan (en organisk kemisk forbindelse) og hører under hovedgruppen carbonhydrider. Det er udelukkende opbygget af enkeltbindinger som en lang kæde. Atomerne sidder her i forhold til hinanden med tetraedervinklen på 109,5˚. Pentan indeholder hydrofobe CH-grupper, der gør molekylet vandafskyende og uopløseligt i vand. Da pentan har symmetrisk ladningsfordeling, skulle man tro, at det ikke kunne blande sig med noget, men der kommer hele tiden overvægt af elektroner, som konstant er i bevægelse i enten den ene eller den anden ende af molekylet. De negative elektroner bevirker, at der opstår en pol i denne ende, og så opstår der selvfølgelig en modsat pol i den anden ende, men fordi elektronerne hele tiden vibrerer, skifter polariseringen konstant. Der opstår altså midlertidige dipoler som påvirker et nabomolekyle, og der sker en ny dipolarisering. Tiltrækningen mellem de skiftende polariseringer er nok til at få et andet upolært stof til at hænge sammen med pentan, og det kan derved gå i forbindelse med andre stoffer. Disse kræfter kaldes londonkræfterne og bindingerne, der bliver dannet hedder londonbindinger. Upolære stoffer er også stoffer, som ikke indeholder grundstoffer med tilstrækkelig stor forskel i elektronegativitet til at danne en positivt elektrisk ladet og en negativt elektrisk ladet ende.
Intermolekylære kræfter[redigér | rediger kildetekst]
Polære molekyler danner især dipol-dipol bindinger, men også nogle gange hydrogenbindinger.
Upolære molekyler danner Londonbindinger.
 Der er for få eller ingen kildehenvisninger i denne artikel, hvilket er et problem. Du kan hjælpe ved at angive troværdige kilder til de påstande, som fremføres i artiklen.
Der er for få eller ingen kildehenvisninger i denne artikel, hvilket er et problem. Du kan hjælpe ved at angive troværdige kilder til de påstande, som fremføres i artiklen.
