Cyankalium
| Cyankalium | ||||
|---|---|---|---|---|
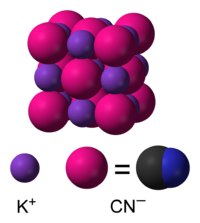
| ||||
| Generelt | ||||
| Systematisk navn | Kaliumcyanid | |||
| Andre navne | Cyankalium | |||
| Molekylformel | KCN | |||
| Molmasse | 65.12 g/mol | |||
| CAS nummer | [151-50-8] | |||
| Egenskaber | ||||
| Massefylde | 1.52 g/cm3 | |||
| Opløselighed i vand | 71.6 g/100 ml (25 °C) | |||
| Smeltepunkt | 634.5 °C | |||
| Kogepunkt | 1625 °C | |||
| Struktur | ||||
| Termokemi | ||||
| Standard molar entropi S |
127.8 J K−1 mol−1 | |||
| Sikkerhed | ||||
| MSDS | ICSC 0671 | |||
| NFPA 704 |
| |||
| R-sætninger | R26/27/28, R32, R50/53 | |||
| S-sætninger | S1/2, S7, S28, S29, S45, S60, S61 | |||
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | ||||
Cyankalium eller kaliumcyanid er en uorganisk forbindelse med formlen KCN. Stoffet er meget giftigt og lugtfri, men pga hydrolyse (og dermed omdannelsen til hydrogencyanid) vil det lugte svagt af bitre mandler, dette er dog genetisk påvirket. Nogle mennesker kan ikke lugte de bitre mandler, mens andre kan. Det bruges blandt andet inden for entomologi i indsamlingskrukker. Der er også meget brugt af bl.a. guldsmede til forsølvning og forgyldning. Under 2.verdenskrig blev det også ofte brugt til selvmord, i form af små piller. Det blev især brugt af modstandsmænd.
| | Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
