Hydronium: Forskelle mellem versioner
Content deleted Content added
Man har ændret navnet på frie H+ ioner fra Protoner til Hydroner da de reagerer meget anderledes kemisk end protoner. |
Nico (diskussion | bidrag) m link |
||
| Linje 4: | Linje 4: | ||
'''Hydronium''' (også kaldet '''oxonium''') er en positivt ladet [[ion (kemi)|ion]], som dannes ud fra vand, når det indeholder [[brint]]-ioner. Formlen er H<sub>3</sub>O<sup>+</sup>. |
'''Hydronium''' (også kaldet '''oxonium''') er en positivt ladet [[ion (kemi)|ion]], som dannes ud fra vand, når det indeholder [[brint]]-ioner. Formlen er H<sub>3</sub>O<sup>+</sup>. |
||
Hydronium opstår, så snart en [[syre]] bliver opløst i vand. De H<sup>+</sup> eller |
Hydronium opstår, så snart en [[syre]] bliver opløst i vand. De H<sup>+</sup> eller [[hydron]]er, som syren frigiver, kan ikke eksistere i fri tilstand. Vandet dissocierer spontant til hydronium- og [[hydroxid]]-ioner under følgende [[kemisk ligevægt|ligevægt]]: |
||
:2H<sub>2</sub>O ↔ H<sub>3</sub>O<sup>+</sup> + OH<sup>−</sup> |
:2H<sub>2</sub>O ↔ H<sub>3</sub>O<sup>+</sup> + OH<sup>−</sup> |
||
Versionen fra 6. maj 2015, 10:09
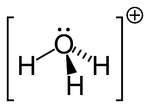


Hydronium (også kaldet oxonium) er en positivt ladet ion, som dannes ud fra vand, når det indeholder brint-ioner. Formlen er H3O+.
Hydronium opstår, så snart en syre bliver opløst i vand. De H+ eller hydroner, som syren frigiver, kan ikke eksistere i fri tilstand. Vandet dissocierer spontant til hydronium- og hydroxid-ioner under følgende ligevægt:
- 2H2O ↔ H3O+ + OH−
OH−-ionens basevirkning afbalancerer syrevirkningen fra hydronium'et, og vandet bibeholder et neutralt pH på 7.0.
