Elektroforese
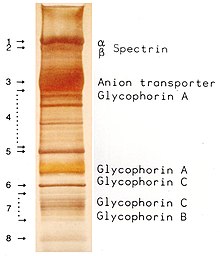


Elektroforese er en biokemisk analysemetode der benyttes til at adskille forskellige molekyler fra hinanden baseret på deres (eller nogle hjælpemolekylers) elektriske egenskaber samt f.eks. størrelse og form.
Analyseopstilling[redigér | rediger kildetekst]
Ved elektroforese adskilles en blanding af stoffer (f.eks. aminosyrer, proteiner, DNA osv.) primært efter deres elektriske ladning. Sekundært kan stofferne også adskilles efter andre molekylære parametre som f.eks. molekylstørrelse. Man kan i princippet udføre elektroforesen i et stykke papir, men det almindeligste er at bruge en såkaldt "gel" der faktisk ligner en plade gele og som kan opfattes som et makromolekylært netværk. Den blanding man vil adskille ("prøven"), anbringes i nogle fordybninger ("slots") i den ene ende (eller evt. i midten) af gelen. Der bliver så etableret et elektrisk felt over gelen, hvorefter ionerne i prøven begynder at vandre alt efter deres ladning, størrelse og form.
Forklaring ved analogi[redigér | rediger kildetekst]
Man kan forestille sig gelen som en kæmpeudgave af et klatrestativ af jernrør som findes på mange legepladser – ca. 2 meter højt, 500 meter langt og med ca. 1,5 meter mellem stængerne. Anbring derpå en flok folkeskoleunger (analogi til "analysen") i den ene ende af stativet og en kasse flødeboller i den anden (analogi til det elektriske felt). Ligesom ionerne bliver tiltrukket af modsat elektrisk ladning, således vil også børnene blive tiltrukket af flødebollerne. De mindste børn vil nå først frem til flødebollerne. Sådan er det også med molekylerne i vores gel: de mindste kommer længst på den tid elektroforesen kører. Man kunne også mene, at de mest sultne børn nok kom først – det svarer til, at ioner med stor elektrisk ladning bliver tiltrukket mest. Dersom man drev analogien videre, så kunne man udføre forsøget med runde, tykke børn i konkurrence med slanke børn af samme vægt. Man ville finde, at de runde og tykke børn ville komme først. Ikke kun fordi de sandsynligvis har et mere hedt forhold til flødeboller end de slanke, men også fordi de slanke jo naturligvis er højere og derfor oftere ramler ind i stængerne. I molekylernes verden betyder dette, at kompakte molekyler kommer længere end de mere langstrakte. Supercoiled DNA kommer f.eks. længere end ikke-supercoiled DNA med samme molekylvægt og ladning.
Andre procesbetingelser[redigér | rediger kildetekst]
Der er mange forskellige variationer over temaet elektroforese. F.eks. kan man fravige princippet om at pH skal være konstant i hele gelen. Ved "Isoelektrisk Fokusering" etablerer man ligefrem en pH-gradient (forklaring af gradient: se Nabla-operatoren) gennem gelen langs det elektriske felt: Højt pH ved – og lavt pH ved +. Det har interesse ved adskillelse af proteiner som har forskellig elektrisk ladning ved forskellige pH-værdier og som har ladningen 0 ved den pH-værdi som vi kalder det "isoelektriske punkt". Ved isoelektrisk fokusering bevæger proteinerne sig altså gennem gelen, indtil de når til deres respektive isoelektriske punkter, hvorefter de ligger stille.
Rumindustri[redigér | rediger kildetekst]
Da tyngdekraften er væsentlig kraftigere end elektroforese-kræfterne, giver det mening at udføre elektroforese i rummet. Tyngdekraften kan skabe bundfald, og overskudsvarme fra de elektrostatiske felter kan skabe konvektion, der kan blande allerede separeret materiale. Separationspotentialet og renhedsgraden ved elektroforese bliver mange gange større i kredsløb.
I 1975 medbragte NASA under Apollo-Sojuz-testprogrammet et elektroforese-eksperiment, der udskilte urokinase (et enzym til behandling af årebetændelse) seks-syv gange bedre end kontroleksperimentet på Jorden.
McDonnell Douglas og Ortho Pharmaceuticals indgik en aftale med NASA om at flyve elektroforese-eksperimenter med rumfærgerne i starten af 1980'erne. McDonnell Douglas fik endda en deres egne forskere, Charles D. Walker, med på tre af flyvningerne.
Det var håbet at ubemandede fabrikssatellitter skulle kunne fremstille medicin ved hjælp af elektroforese; beta-celler (mod diabetes), interferoner (mod cancer), antitrypsin (mod lungeemfysem), væksthormoner og midler mod hæmofili og brandsår[2].
Typiske elektroforesetyper[redigér | rediger kildetekst]
- SDS-PAGE, SDS-polyacrylamid-elektroforese
- Kapillær-elektroforese, en:Capillary electrophoresis
- Agarose-gelelektroforese, de:Agarose-Gelelektrophorese
- Todimensionel gelelektroforese, se f.eks. de:Immunelektrophorese
- Immunelektroforese, en:Immunoelectrophoresis
- Affinitetselektroforese, en:Affinity electrophoresis
Se også[redigér | rediger kildetekst]
Kilder[redigér | rediger kildetekst]
- ^ Hempelmann E, Götze O (1984). "Characterization of membrane proteins by polychromatic silver staining". Hoppe Seyler's Z Physiol Chem. 365: 241-242.
- ^ Erik Tandberg: Romfergen – på vei mot en ny tidsalder, 1983, Universitetsforlaget, ISBN 82-00-06263-5
