Aldehyd
 |
 |
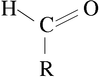
Et aldehyd er både betegnelsen for den organiske funktionelle gruppe bestående af en carbonylgruppe, som er bundet til et H-atom (RCHO) og til en gruppe, der enten kan være endnu et H-atom eller et organisk radikal, og kemiske forbindelser, der indeholder en sådan gruppe. De fleste sukre er aldehyder eller derivater deraf, som regel hemiacetaler eller acetaler. Det mest simple aldehyd er formaldehyd (IUPAC-navn methanal):
[redigér | rediger kildetekst]
Aldehyder kan navngives på to måder: ved at tilføje endelsen -al til navnet på den tilsvarende alkan, alken eller alkyn; eller ved at tilføje -carbaldehyd til navnet på forbindelsen, hvor aldehydgruppen er skiftet ud med H. Et eksempel på det første er methanal, CH2O, der er navngivet ud fra methan, CH4, et eksempel på det andet er cyclohexancarbaldehyd, c-C6H11CHO, det er navngivet ud fra cyclohexan.
Kemiske egenskaber[redigér | rediger kildetekst]

Carbonylgruppen er polær, hvilket gør at aldehyder smelter og koger højere end de tilsvarende alkaner, og at de er mere opløselige i vand. I vandig opløsning forefindes aldehyder normalt på hydratiseret form som geminale dioler, dvs RCH(OH)2.
Reaktioner[redigér | rediger kildetekst]
Fremstilling[redigér | rediger kildetekst]
Aldehyder fremstilles som regel på en af fire måder:
- Delvis oxidation af en primær alkohol
- Delvis reduktion af et syrederivat
- Spaltning af en alken med reduktiv ozonolyse
- Hydroformylering af en alken med CO og H2
Ved oxidationen kræves specielle omstændigheder for at undgå oxidation til syre. Dette gøres som regel under vandfrie omstændigheder.
Nukleophile additioner[redigér | rediger kildetekst]
- Aldehyd + nukleophil → tetraedrisk additionsprodukt
- Aldehyd + alkohol + katalytisk syre el. katalytisk base → hemiacetal
- Hemiacetal + alkohol + katalytisk syre → acetal
- Aldehyd + NaBH4 → alkohol
- Aldehyd + RMgX (Grignardreagens) → magnesiumalkoholat
- magnesiumalkoholat + H2O → sekundær alkohol
- Aldehyd + H2O → hydrat
- Denne ligevægt er som regel forskudt mod venstre, men formaldehyd og aldehyder med elektrontiltrækkende grupper (eksempelvis chloral, CCl3CHO) findes som hydrater i vandig opløsning.
Keto-enol tautomeriseringen[redigér | rediger kildetekst]
Aldehyder med et eller flere α-H'er, dvs. H-atomer på kulstofatomet ved siden af carbonylgruppen, kan tautomerisere til enoler, enten syre- eller basekatalyseret. Enoler og især de tilsvarende anioner, enolater, er nukleofile på α-C'et. α-H'et har en pKa-værdi på 20 i simple aldehyder.
Aldolkondensationen[redigér | rediger kildetekst]
- Aldehyd + base → enolat
- Aldehyd + Enolat → aldol
- Aldol → α-β-umættet aldehyd + H2O
Andre reaktioner[redigér | rediger kildetekst]
- Aldehyder oxideres nemt til carboxylsyrer, både af oxiderende stoffer som permanganationen og chrom(VI)oxid, og af luftens ilt. De fleste aldehyder er derfor ikke stabile i luft, men omdannes langsomt til den tilsvarende carboxylsyre
