Bicarbonat
| Bicarbonat | |
|---|---|
 | |
 | |
| Generelt | |
| Systematisk navn | Hydroxidodioxidocarbonat(1−) |
| Andre navne | Bikarbonat Hydrogencarbonat Hydrogenkarbonat |
| Molekylformel | HCO3- |
| Molarmasse | 61,0168 g/mol |
| CAS-nummer | |
| PubChem | |
| SMILES | OC([O-])=O |
| Kemiske egenskaber | |
| Syrestyrkekonstant (pKa) | 10,32 (Carbonats korresponderende syre)[1] |
| Basestyrkekonstant (pKb) | 7,63 (Kulsyres korresponderende base)[1] |
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |
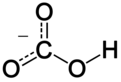
Bicarbonat (RO: Bikarbonat) er trivialnavnet for den fleratomige anion HCO3-. Det systematiske navn ifølge IUPAC er hydrogencarbonat.[2] Bicarbonat er kulsyres korresponderende base. Salte, der indeholder bicarbonat, betegnes bicarbonater eller hydrogencarbonater.
Bicarbonat spiller en afgørende rolle i bevarelsen af menneskekroppens homøostase, idet bicarbonat sammen med kulsyre danner et buffersystem, der holder blodets pH på mellem 7,36 og 7,42 (hvilket er essentielt for, at kroppen kan varetage sine normale funktioner).[3]
Navnet "bicarbonat" blev opfundet af den engelske kemiker William Hyde Wollaston i 1814.[4] Præfikset "bi-" stammer fra et forældet navngivningssystem og skyldes, at der i natriumhydrogencarbonat (NaHCO3) og andre bicarbonater er dobbelt så meget karbonat (CO2−3) pr. Na+-ion som i natriumkarbonat (Na2CO3) og andre karbonater.[5] Navnet bruges fortsat som trivialnavn.
Referencer
[redigér | rediger kildetekst]- ^ a b Andersen, Erik Strandgaard; Jespergaard, Paul; Østergaard, Ove Grønbæk. DATABOG fysik kemi, 11. udgave, pp. 66-67. København: F & K forlaget, 2009. ISBN 978-87-87229-61-6.
- ^ Nomenclature of Inorganic Chemistry IUPAC Recommendations 2005 (PDF), IUPAC, s. 137. (engelsk)
- ^ "Clinical correlates of pH levels: bicarbonate as a buffer". Biology.arizona.edu. oktober 2006. (engelsk)
- ^ William Hyde Wollaston (1814). "A synoptic scale of chemical equivalents", Philosophical Transactions of the Royal Society, 104: 1-22. Wollaston anvender betegnelsen "bicarbonat" på side 11: "The next question that occurs relates to the composition of this crystallized carbonate of potash, which I am induced to call bi-carbonate of potash, for the purpose of marking more decidedly the distinction between this salt and that which is commonly called a subcarbonate, and in order to refer at once to the double dose of carbonic acid contained in it." (engelsk)
- ^ "Ask a scientist" (Webside ikke længere tilgængelig). Sponseret og drevet af Argonne National Laboratory. Besøgt 19. august 2016. (engelsk)
