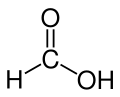
Myresyre
Udseende
| Myresyre | |||
|---|---|---|---|
| IUPAC-navn Methansyre | |||
| Generelt | |||
| Systematisk navn | Methansyre | ||
| Molekylformel | HCOOH | ||
| Molarmasse | 46,03 g/mol | ||
| Fremtræden | farveløs væske | ||
| CAS-nummer | |||
| Kemiske egenskaber | |||
| Massefylde | 1,220 g/mL 3 | ||
| Opløselighed i vand | blandbar | ||
| Smeltepunkt | 8,4 °C | ||
| Kogepunkt | 100,8 °C | ||
| Syrestyrkekonstant (pKa) | 3,77 | ||
| Refraktionsindeks | 1,3714 (20 °C) | ||
| Viskositet | 1,57 cP ved 268 °C | ||
| Beslægtede stoffer | |||
| Andre carboxylsyrer | Eddikesyre Propionsyre | ||
| Relaterede forbindelser | Formaldehyd Methanol | ||
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |||
Myresyre, også kaldet methansyre, er den mest simple alifatiske carboxylsyre og har konstitutionsformlen HCOOH.
Myresyre kan fremstilles ved oxidation af formaldehyd ved tilstedeværelse af en stærk base. To formaldehydmolekyler reagerer med hinanden, hvorved der dannes methanol og anionen af myresyre. Dette sker ved den såkaldte Cannizzarroreaktion.
Eksterne kilder/henvisninger[redigér | rediger kildetekst]
| | Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |