Spændingsrækken: Forskelle mellem versioner
Har givet reaktionen dets rette navn. |
Wikilink |
||
| Linje 6: | Linje 6: | ||
Hvis et bestemt stof "A" fra spændingsrækken indgår i en kemisk forbindelse, vil denne forbindelse reagere med ethvert stof "B" der står til venstre for stof "A" i spændingsrækken: Ved reaktionen udskilles stof "A" i ren form fra den kemiske forbindelse, og det mindre "ædle" stof "B" overtager "A's" plads i forbindelsen. Et særligt eksempel på dette er [[syre]]r, hvis kendetegn er deres tilbøjelighed til at levere brintioner til omgivelserne: Ethvert metal til venstre for brints plads i spændingsrækken kan opløses i en [[syre]], hvorved brinten fra syren udskilles som [[gas]] mens metallet overtager brintens "plads" i syren, og danner et [[Salt (kemi)|salt]] sammen med [[syrerest]]en. |
Hvis et bestemt stof "A" fra spændingsrækken indgår i en kemisk forbindelse, vil denne forbindelse reagere med ethvert stof "B" der står til venstre for stof "A" i spændingsrækken: Ved reaktionen udskilles stof "A" i ren form fra den kemiske forbindelse, og det mindre "ædle" stof "B" overtager "A's" plads i forbindelsen. Et særligt eksempel på dette er [[syre]]r, hvis kendetegn er deres tilbøjelighed til at levere brintioner til omgivelserne: Ethvert metal til venstre for brints plads i spændingsrækken kan opløses i en [[syre]], hvorved brinten fra syren udskilles som [[gas]] mens metallet overtager brintens "plads" i syren, og danner et [[Salt (kemi)|salt]] sammen med [[syrerest]]en. |
||
På grund af deres reaktionsvillighed iltes eller "ruster" metaller i den venstre ende af spændingsrækken generelt meget let, men [[aluminium]] bryder tilsyneladende denne regel, og bevarer en blank og tilsyneladende ikke synderlig "iltet" metaloverflade. Det skyldes det lag af [[aluminiumoxid]] der dannes ved oxideringen af aluminium; en ca. 3 [[mikrometer]] tynd men særdeles slidstærk "hinde" dannes på |
På grund af deres reaktionsvillighed iltes eller "ruster" metaller i den venstre ende af spændingsrækken generelt meget let, men [[aluminium]] bryder tilsyneladende denne regel, og bevarer en blank og tilsyneladende ikke synderlig "iltet" metaloverflade. Det skyldes det lag af [[aluminiumoxid]] der dannes ved oxideringen af aluminium; en ca. 3 [[mikrometer]] tynd men særdeles slidstærk "hinde" dannes på overflade af metallet, hvilket beskytter resten af metaller under dette lag. Denne proces kaldes [[passivering]]. |
||
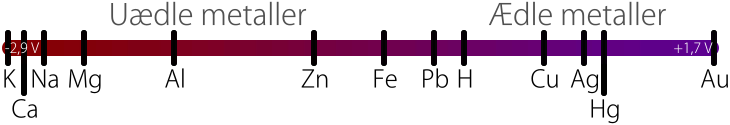
[[Billede:Spaendingsraekke.svg|center|Den forenklede spændingsrække]] |
[[Billede:Spaendingsraekke.svg|center|Den forenklede spændingsrække]] |
||
''<center>Den forenklede spændingsrække</center>'' |
''<center>Den forenklede spændingsrække</center>'' |
||
==Se også== |
==Se også== |
||
Versionen fra 22. jan. 2020, 10:10
Spændingsrækken er en række af grundstoffer; brint samt metallerne, sorteret efter deres reaktionsvillighed: Metallerne i den venstre ende af rækken danner lettere kemiske forbindelser med andre stoffer, end metaller der står længere mod højre. Man taler undertiden om de nævnte metallers ædelhed, hvor de lidet reaktionsvillige stoffer sidst i rækken omtales som "ædle"; fordi de ikke gerne går i forbindelse med andre stoffer, kan man finde disse såkaldt ædle stoffer i ren, metallisk form i naturen.
Spændingsrækken for de mest almindelige metaller, ordnet efter faldende reaktionsvillighed, lyder:
Hvis et bestemt stof "A" fra spændingsrækken indgår i en kemisk forbindelse, vil denne forbindelse reagere med ethvert stof "B" der står til venstre for stof "A" i spændingsrækken: Ved reaktionen udskilles stof "A" i ren form fra den kemiske forbindelse, og det mindre "ædle" stof "B" overtager "A's" plads i forbindelsen. Et særligt eksempel på dette er syrer, hvis kendetegn er deres tilbøjelighed til at levere brintioner til omgivelserne: Ethvert metal til venstre for brints plads i spændingsrækken kan opløses i en syre, hvorved brinten fra syren udskilles som gas mens metallet overtager brintens "plads" i syren, og danner et salt sammen med syreresten.
På grund af deres reaktionsvillighed iltes eller "ruster" metaller i den venstre ende af spændingsrækken generelt meget let, men aluminium bryder tilsyneladende denne regel, og bevarer en blank og tilsyneladende ikke synderlig "iltet" metaloverflade. Det skyldes det lag af aluminiumoxid der dannes ved oxideringen af aluminium; en ca. 3 mikrometer tynd men særdeles slidstærk "hinde" dannes på overflade af metallet, hvilket beskytter resten af metaller under dette lag. Denne proces kaldes passivering.
Se også
| | Spire Denne naturvidenskabsartikel er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
