Bruger:Metalindustrien/grundstof: Forskelle mellem versioner
| Linje 33: | Linje 33: | ||
Sølv reagerer ikke med luft, selv ved rød varme, og blev derfor af [[alkymist]]er anset som et [[ædelmetal]] på linje med [[guld]]. Dets reaktivitet ligger mellem kobbers (som danner [[kobber(I)oxid]] når det opvarmes i luften til rød varme) og gulds. Sølv reagerer, ligesom kobber, med [[svovl]] og dets forbindelser, som misfarver det i luften og danner [[sølvsulfid]] (kobber danner i stedet det grønne [[sulfat]], mens guld slet ikke reagerer). I modsætning til kobber så vil sølv ikke reagere med [[halogen]]er, med undtagelse af [[fluor]]gas, som det danner [[sølv(II)fluorid|difluorid]] med. Selvom sølv ikke angribes af ikke-oxiderende syrer så vil det stadig kunne opløses i varm, koncentreret [[svovlsyre]], såvel som i fortyndet eller koncentreret [[salpetersyre]]. Ved tilstedeværelsen af luft, og især ved tilstedeværelsen af [[brintoverilte]], vil sølv nemt opløses i vandige opløsninger af [[cyanid]].<ref name=Greenwood1179>Greenwood and Earnshaw, p. 1179</ref> |
Sølv reagerer ikke med luft, selv ved rød varme, og blev derfor af [[alkymist]]er anset som et [[ædelmetal]] på linje med [[guld]]. Dets reaktivitet ligger mellem kobbers (som danner [[kobber(I)oxid]] når det opvarmes i luften til rød varme) og gulds. Sølv reagerer, ligesom kobber, med [[svovl]] og dets forbindelser, som misfarver det i luften og danner [[sølvsulfid]] (kobber danner i stedet det grønne [[sulfat]], mens guld slet ikke reagerer). I modsætning til kobber så vil sølv ikke reagere med [[halogen]]er, med undtagelse af [[fluor]]gas, som det danner [[sølv(II)fluorid|difluorid]] med. Selvom sølv ikke angribes af ikke-oxiderende syrer så vil det stadig kunne opløses i varm, koncentreret [[svovlsyre]], såvel som i fortyndet eller koncentreret [[salpetersyre]]. Ved tilstedeværelsen af luft, og især ved tilstedeværelsen af [[brintoverilte]], vil sølv nemt opløses i vandige opløsninger af [[cyanid]].<ref name=Greenwood1179>Greenwood and Earnshaw, p. 1179</ref> |
||
Historiske [[Artefakt (arkæologi)|sølvartefakter]] er typisk blevet forringet på tre primære måder: misfarvning, dannelse af [[sølvklorid]] pga. længerevarende nedsænkning i saltvand samt gennem reaktioner med [[nitrat]]ioner eller ilt. Frisk sølvklorid er bleggylt og bliver lilla ved at blive udsat for lys; det projicerer en smule fra artefaktens overflade. [[Udfældning]]en af kobber i oldtidens sølv kan anvendes til at datere artefakter, da kobber næsten altid er en bestanddel i [[legering|sølvlegeringer]].<ref>[https://web.archive.org/web/20130509014548/http://events.nace.org/library/corrosion/Artifacts/silver.asp "Silver Artifacts"] in ''Corrosion – Artifacts''. NACE Resource Center</ref> |
Historiske [[Artefakt (arkæologi)|sølvartefakter]] er typisk blevet forringet på tre primære måder: misfarvning, dannelse af [[sølvklorid]] pga. længerevarende nedsænkning i saltvand samt gennem reaktioner med [[nitrat]]ioner eller ilt. Frisk sølvklorid er bleggylt og bliver lilla ved at blive udsat for lys; det projicerer en smule fra artefaktens overflade. [[Fældning (kemi)|Udfældning]]en af kobber i oldtidens sølv kan anvendes til at datere artefakter, da kobber næsten altid er en bestanddel i [[legering|sølvlegeringer]].<ref>[https://web.archive.org/web/20130509014548/http://events.nace.org/library/corrosion/Artifacts/silver.asp "Silver Artifacts"] in ''Corrosion – Artifacts''. NACE Resource Center</ref> |
||
Sølvmetal kan angribes af stærke oxidationsmidler såsom [[kaliumpermanganat]] ({{chem|KMnO|4}}) og [[kaliumdichromat]] ({{chem|K|2|Cr|2|O|7}}), samt ved tilstedeværelsen af [[kaliumbromid]] ({{chem|KBr}}). Disse forbindelser anvendes indenfor [[fotografering]] til at [[blegning|blege]] sølvbilleder idet man konverterer dem til sølvbromid, der enten kan fastsættes med [[thiosulfat]] eller genudvikles og dermed intensivere det oprindelige billede. Sølv danner [[cyanid]]komplekser ([[sølvcyanid]]), der er opløselige i vand ved tilstedeværelsen af et overskud af cyanidioner. Sølvcyanidopløsninger kan anvendes til [[galvanisering]] af sølv.<ref name=photo>{{cite book| pages = [https://archive.org/details/silverhalidereco00bjel/page/n172 156]–66| title=Silver-halide recording materials: for holography and their processing| url = https://archive.org/details/silverhalidereco00bjel| url-access = limited| last = Bjelkhagen |first=Hans I.| publisher= Springer| date =1995| isbn = 978-3-540-58619-7}}</ref> |
Sølvmetal kan angribes af stærke oxidationsmidler såsom [[kaliumpermanganat]] ({{chem|KMnO|4}}) og [[kaliumdichromat]] ({{chem|K|2|Cr|2|O|7}}), samt ved tilstedeværelsen af [[kaliumbromid]] ({{chem|KBr}}). Disse forbindelser anvendes indenfor [[fotografering]] til at [[blegning|blege]] sølvbilleder idet man konverterer dem til sølvbromid, der enten kan fastsættes med [[thiosulfat]] eller genudvikles og dermed intensivere det oprindelige billede. Sølv danner [[cyanid]]komplekser ([[sølvcyanid]]), der er opløselige i vand ved tilstedeværelsen af et overskud af cyanidioner. Sølvcyanidopløsninger kan anvendes til [[galvanisering]] af sølv.<ref name=photo>{{cite book| pages = [https://archive.org/details/silverhalidereco00bjel/page/n172 156]–66| title=Silver-halide recording materials: for holography and their processing| url = https://archive.org/details/silverhalidereco00bjel| url-access = limited| last = Bjelkhagen |first=Hans I.| publisher= Springer| date =1995| isbn = 978-3-540-58619-7}}</ref> |
||
Versionen fra 30. maj 2021, 15:02
Kemiske egenskaber
| Oxideringstrin | Koordinationstal | Stereokemi | Repræsentativ forbindelse |
|---|---|---|---|
| 0 (d10s1) | 3 | Plan | Ag(CO)3 |
| 1 (d10) | 2 | Lineær | [Ag(CN)2]− |
| 3 | Trigonal plan | AgI(PEt2Ar)2 | |
| 4 | Tetrahedral | [Ag(diars)2]+ | |
| 6 | Octahedral | AgF, AgCl, AgBr | |
| 2 (d9) | 4 | Firkantet plan | [Ag(py)4]2+ |
| 3 (d8) | 4 | Firkantet plan | [AgF4]− |
| 6 | Octahedral | [AgF6]3− |
Sølv er et relativt ureaktivt metal, da dets fyldte 4d-skal ikke er særligt effektiv til at skærme de elektrostatiske tiltrækningskrafter fra kernen til den yderstliggende 5s-elektron, og sølv er derfor placeret nær bunden af den elektrokemiske serie (E0(Ag+/Ag) = +0.799 V).[2] I gruppe 11 har sølv den laveste førsteioniseringsenergi (hvilket viser 5s-orbitalens ustabilitet), men har højere anden- og tredjeioniseringsenergier end kobber og guld (hvilket viser 4d-orbitalernes stabilitet), og sølvets kemi er derfor hovedsageligt i et oxidationstrin på +1, hvilket viser det gradvist mere begrænsede interval af oxidationstrin langs overgangsserien, da d-orbitalerne fyldes og stabiliseres.[3] For kobber forklarer Cu2+'s store hydrationsenergi sammenlignet med Cu+ hvorfor den førstnævnte er mere stabil i vandholdige opløsninger og fastform på trods af manglen på sidstnævntes stabile, fyldte d-underskal. I sølv bliver denne effekt dog tilsidesat af dets store andenioniseringsenergi, og følgelig er Ag+ den stabile art i vandige opløsninger og fastform, mens Ag2+ er meget mindre stabil, da den oxiderer vand.[3]
De fleste sølvforbindelser har tydelige kovalente egenskaber på grund af sølvs lille størrelse og høje første ioniseringsenergi (730,8 kJ/mol).[2] Derudover er sølvs Pauling-elektronegativitet på 1,93 højere end blys (1,87) og dets elektronaffinitet på 125,6 kJ/mol er meget højere end brints (72,8 kJ/mol) og kun lidt under ilts (141,0 kJ/mol).[4] På grund af dets fulde d-underskal udviser sølv i dets primære +1-oxidationstrin relativt få egenskaber fra de egentlige overgangsmetaller fra gruppe 4 til 10, danner relativt ustabile metalorganiske forbindelser, danner lineære komplekser, der viser meget lave koordinationstal såsom 2, samt danner et amfotært oxid[5] såvel som Zintl-faser ligesom andre metaller.[6] Sølvs +1-oxidationstrin er, i modsætning til de foregående overgangsmetaller, stabilt selv i manglen på π-acceptorligander.[3]
Sølv reagerer ikke med luft, selv ved rød varme, og blev derfor af alkymister anset som et ædelmetal på linje med guld. Dets reaktivitet ligger mellem kobbers (som danner kobber(I)oxid når det opvarmes i luften til rød varme) og gulds. Sølv reagerer, ligesom kobber, med svovl og dets forbindelser, som misfarver det i luften og danner sølvsulfid (kobber danner i stedet det grønne sulfat, mens guld slet ikke reagerer). I modsætning til kobber så vil sølv ikke reagere med halogener, med undtagelse af fluorgas, som det danner difluorid med. Selvom sølv ikke angribes af ikke-oxiderende syrer så vil det stadig kunne opløses i varm, koncentreret svovlsyre, såvel som i fortyndet eller koncentreret salpetersyre. Ved tilstedeværelsen af luft, og især ved tilstedeværelsen af brintoverilte, vil sølv nemt opløses i vandige opløsninger af cyanid.[1]
Historiske sølvartefakter er typisk blevet forringet på tre primære måder: misfarvning, dannelse af sølvklorid pga. længerevarende nedsænkning i saltvand samt gennem reaktioner med nitrationer eller ilt. Frisk sølvklorid er bleggylt og bliver lilla ved at blive udsat for lys; det projicerer en smule fra artefaktens overflade. Udfældningen af kobber i oldtidens sølv kan anvendes til at datere artefakter, da kobber næsten altid er en bestanddel i sølvlegeringer.[7]
Sølvmetal kan angribes af stærke oxidationsmidler såsom kaliumpermanganat (KMnO4) og kaliumdichromat (K2Cr2O7), samt ved tilstedeværelsen af kaliumbromid (KBr). Disse forbindelser anvendes indenfor fotografering til at blege sølvbilleder idet man konverterer dem til sølvbromid, der enten kan fastsættes med thiosulfat eller genudvikles og dermed intensivere det oprindelige billede. Sølv danner cyanidkomplekser (sølvcyanid), der er opløselige i vand ved tilstedeværelsen af et overskud af cyanidioner. Sølvcyanidopløsninger kan anvendes til galvanisering af sølv.[8]
Sølvs mest udbredte oxidationstrin er (fra mest til mindst udbredt): +1 (den mest stabile tilstand; for eksempel sølvnitrat, AgNO3); +2 (stærkt oxiderende; for eksempel sølv(II)fluorid, AgF2); og meget sjældent +3 (ekstremt oxiderende; for eksempel kaliumtetrafluoroargentat(III), KAgF4).[9] +1-tilstanden er langt den mest udbredte, fulgt af den let reducerbare +2-tilstand. For at opnå +3-tilstanden kræve meget stærke oxidationsmidler såsom fluor eller peroxodisulfat, og nogle sølv(III)forbindelser reagerer med atmosfærisk fugt og angriber glas.[10] Sølv(III)fluorid opnås normalt ved at få sølv eller sølvmonofluorid til at reagere med det stærkeste kendte oxidationsmiddel, kryptondifluorid.[11]
Compounds
Oxides and chalcogenides

Silver and gold have rather low chemical affinities for oxygen, lower than copper, and it is therefore expected that silver oxides are thermally quite unstable. Soluble silver(I) salts precipitate dark-brown silver(I) oxide, Ag2O, upon the addition of alkali. (The hydroxide AgOH exists only in solution; otherwise it spontaneously decomposes to the oxide.) Silver(I) oxide is very easily reduced to metallic silver, and decomposes to silver and oxygen above 160 °C.[12] This and other silver(I) compounds may be oxidized by the strong oxidizing agent peroxodisulfate to black AgO, a mixed silver(I,III) oxide of formula AgIAgIIIO2. Some other mixed oxides with silver in non-integral oxidation states, namely Ag2O3 and Ag3O4, are also known, as is Ag3O which behaves as a metallic conductor.[12]
Silver(I) sulfide, Ag2S, is very readily formed from its constituent elements and is the cause of the black tarnish on some old silver objects. It may also be formed from the reaction of hydrogen sulfide with silver metal or aqueous Ag+ ions. Many non-stoichiometric selenides and tellurides are known; in particular, AgTe~3 is a low-temperature superconductor.[12]
Halides
The only known dihalide of silver is the difluoride, AgF2, which can be obtained from the elements under heat. A strong yet thermally stable and therefore safe fluorinating agent, silver(II) fluoride is often used to synthesize hydrofluorocarbons.[13]
In stark contrast to this, all four silver(I) halides are known. The fluoride, chloride, and bromide have the sodium chloride structure, but the iodide has three known stable forms at different temperatures; that at room temperature is the cubic zinc blende structure. They can all be obtained by the direct reaction of their respective elements.[13] As the halogen group is descended, the silver halide gains more and more covalent character, solubility decreases, and the color changes from the white chloride to the yellow iodide as the energy required for ligand-metal charge transfer (X−Ag+ → XAg) decreases.[13] The fluoride is anomalous, as the fluoride ion is so small that it has a considerable solvation energy and hence is highly water-soluble and forms di- and tetrahydrates.[13] The other three silver halides are highly insoluble in aqueous solutions and are very commonly used in gravimetric analytical methods.[14] All four are photosensitive (though the monofluoride is so only to ultraviolet light), especially the bromide and iodide which photodecompose to silver metal, and thus were used in traditional photography.[13] The reaction involved is:[15]
- X− + hν → X + e− (excitation of the halide ion, which gives up its extra electron into the conduction band)
- Ag+ + e− → Ag (liberation of a silver ion, which gains an electron to become a silver atom)
The process is not reversible because the silver atom liberated is typically found at a crystal defect or an impurity site, so that the electron's energy is lowered enough that it is "trapped".[15]
Other inorganic compounds

White silver nitrate, AgNO3, is a versatile precursor to many other silver compounds, especially the halides, and is much less sensitive to light. It was once called lunar caustic because silver was called luna by the ancient alchemists, who believed that silver was associated with the moon.[16] It is often used for gravimetric analysis, exploiting the insolubility of the heavier silver halides which it is a common precursor to.[14] Silver nitrate is used in many ways in organic synthesis, e.g. for deprotection and oxidations. Ag+ binds alkenes reversibly, and silver nitrate has been used to separate mixtures of alkenes by selective absorption. The resulting adduct can be decomposed with ammonia to release the free alkene.[17]
Yellow silver carbonate, Ag2CO3 can be easily prepared by reacting aqueous solutions of sodium carbonate with a deficiency of silver nitrate.[18] Its principal use is for the production of silver powder for use in microelectronics. It is reduced with formaldehyde, producing silver free of alkali metals:[19]
- Ag2CO3 + CH2O → 2 Ag + 2 CO2 + H2
Silver carbonate is also used as a reagent in organic synthesis such as the Koenigs-Knorr reaction. In the Fétizon oxidation, silver carbonate on celite acts as an oxidising agent to form lactones from diols. It is also employed to convert alkyl bromides into alcohols.[18]
Silver fulminate, AgCNO, a powerful, touch-sensitive explosive used in percussion caps, is made by reaction of silver metal with nitric acid in the presence of ethanol. Other dangerously explosive silver compounds are silver azide, AgN3, formed by reaction of silver nitrate with sodium azide,[20] and silver acetylide, Ag2C2, formed when silver reacts with acetylene gas in ammonia solution.[3] In its most characteristic reaction, silver azide decomposes explosively, releasing nitrogen gas: given the photosensitivity of silver salts, this behaviour may be induced by shining a light on its crystals.[3]
- 2 AgN3 (s) → 3 N2 (g) + 2 Ag (s)
Coordination compounds
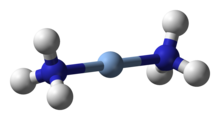
Silver complexes tend to be similar to those of its lighter homologue copper. Silver(III) complexes tend to be rare and very easily reduced to the more stable lower oxidation states, though they are slightly more stable than those of copper(III). For instance, the square planar periodate [Ag(IO5OH)2]5− and tellurate [Ag{TeO4(OH)2}2]5− complexes may be prepared by oxidising silver(I) with alkaline peroxodisulfate. The yellow diamagnetic [AgF4]− is much less stable, fuming in moist air and reacting with glass.[10]
Silver(II) complexes are more common. Like the valence isoelectronic copper(II) complexes, they are usually square planar and paramagnetic, which is increased by the greater field splitting for 4d electrons than for 3d electrons. Aqueous Ag2+, produced by oxidation of Ag+ by ozone, is a very strong oxidising agent, even in acidic solutions: it is stabilized in phosphoric acid due to complex formation. Peroxodisulfate oxidation is generally necessary to give the more stable complexes with heterocyclic amines, such as [Ag(py)4]2+ and [Ag(bipy)2]2+: these are stable provided the counterion cannot reduce the silver back to the +1 oxidation state. [AgF4]2− is also known in its violet barium salt, as are some silver(II) complexes with N- or O-donor ligands such as pyridine carboxylates.[21]
By far the most important oxidation state for silver in complexes is +1. The Ag+ cation is diamagnetic, like its homologues Cu+ and Au+, as all three have closed-shell electron configurations with no unpaired electrons: its complexes are colourless provided the ligands are not too easily polarized such as I−. Ag+ forms salts with most anions, but it is reluctant to coordinate to oxygen and thus most of these salts are insoluble in water: the exceptions are the nitrate, perchlorate, and fluoride. The tetracoordinate tetrahedral aqueous ion [Ag(H2O)4]+ is known, but the characteristic geometry for the Ag+ cation is 2-coordinate linear. For example, silver chloride dissolves readily in excess aqueous ammonia to form [Ag(NH3)2]+; silver salts are dissolved in photography due to the formation of the thiosulfate complex [Ag(S2O3)2]3−; and cyanide extraction for silver (and gold) works by the formation of the complex [Ag(CN)2]−. Silver cyanide forms the linear polymer {Ag–C≡N→Ag–C≡N→}; silver thiocyanate has a similar structure, but forms a zigzag instead because of the sp3-hybridized sulfur atom. Chelating ligands are unable to form linear complexes and thus silver(I) complexes with them tend to form polymers; a few exceptions exist, such as the near-tetrahedral diphosphine and diarsine complexes [Ag(L–L)2]+.[22]
Organometallic
Under standard conditions, silver does not form simple carbonyls, due to the weakness of the Ag–C bond. A few are known at very low temperatures around 6–15 K, such as the green, planar paramagnetic Ag(CO)3, which dimerizes at 25–30 K, probably by forming Ag–Ag bonds. Additionally, the silver carbonyl [Ag(CO)] [B(OTeF5)4] is known. Polymeric AgLX complexes with alkenes and alkynes are known, but their bonds are thermodynamically weaker than even those of the platinum complexes (though they are formed more readily than those of the analogous gold complexes): they are also quite unsymmetrical, showing the weak π bonding in group 11. Ag–C σ bonds may also be formed by silver(I), like copper(I) and gold(I), but the simple alkyls and aryls of silver(I) are even less stable than those of copper(I) (which tend to explode under ambient conditions). For example, poor thermal stability is reflected in the relative decomposition temperatures of AgMe (−50 °C) and CuMe (−15 °C) as well as those of PhAg (74 °C) and PhCu (100 °C).[23]
The C–Ag bond is stabilized by perfluoroalkyl ligands, for example in AgCF(CF3)2.[24] Alkenylsilver compounds are also more stable than their alkylsilver counterparts.[25] Silver-NHC complexes are easily prepared, and are commonly used to prepare other NHC complexes by displacing labile ligands. For example, the reaction of the bis(NHC)silver(I) complex with bis(acetonitrile)palladium dichloride or chlorido(dimethyl sulfide)gold(I):[26]
Intermetallic

Silver forms alloys with most other elements on the periodic table. The elements from groups 1–3, except for hydrogen, lithium, and beryllium, are very miscible with silver in the condensed phase and form intermetallic compounds; those from groups 4–9 are only poorly miscible; the elements in groups 10–14 (except boron and carbon) have very complex Ag–M phase diagrams and form the most commercially important alloys; and the remaining elements on the periodic table have no consistency in their Ag–M phase diagrams. By far the most important such alloys are those with copper: most silver used for coinage and jewellery is in reality a silver–copper alloy, and the eutectic mixture is used in vacuum brazing. The two metals are completely miscible as liquids but not as solids; their importance in industry comes from the fact that their properties tend to be suitable over a wide range of variation in silver and copper concentration, although most useful alloys tend to be richer in silver than the eutectic mixture (71.9% silver and 28.1% copper by weight, and 60.1% silver and 28.1% copper by atom).[27]
Most other binary alloys are of little use: for example, silver–gold alloys are too soft and silver–cadmium alloys too toxic. Ternary alloys have much greater importance: dental amalgams are usually silver–tin–mercury alloys, silver–copper–gold alloys are very important in jewellery (usually on the gold-rich side) and have a vast range of hardnesses and colours, silver–copper–zinc alloys are useful as low-melting brazing alloys, and silver–cadmium–indium (involving three adjacent elements on the periodic table) is useful in nuclear reactors because of its high thermal neutron capture cross-section, good conduction of heat, mechanical stability, and resistance to corrosion in hot water.[27]
Etymology
The word "silver" appears in Old English in various spellings, such as seolfor and siolfor. It is cognate with Old High German silabar; Gothic silubr; or Old Norse silfr, all ultimately deriving from Proto-Germanic *silubra. The Balto-Slavic words for silver are rather similar to the Germanic ones (e.g. Russian серебро [serebró], Polish srebro, Lithuanian sidãbras), as is the Celtiberian form silabur. They may have a common Indo-European origin, although their morphology rather suggest a non-Indo-European Wanderwort.[28][29] Some scholars have thus proposed a Paleo-Hispanic origin, pointing to the Basque form zilharr as an evidence.[30]
The chemical symbol Ag is from the Latin word for "silver", argentum (compare Ancient Greek ἄργυρος, árgyros), from the Proto-Indo-European root *h₂erǵ- (formerly reconstructed as *arǵ-), meaning "white" or "shining". This was the usual Proto-Indo-European word for the metal, whose reflexes are missing in Germanic and Balto-Slavic.[29]
History

Silver was one of the seven metals of antiquity that were known to prehistoric humans and whose discovery is thus lost to history.[31] In particular, the three metals of group 11, copper, silver, and gold, occur in the elemental form in nature and were probably used as the first primitive forms of money as opposed to simple bartering.[32] However, unlike copper, silver did not lead to the growth of metallurgy on account of its low structural strength, and was more often used ornamentally or as money.[33] Since silver is more reactive than gold, supplies of native silver were much more limited than those of gold.[32] For example, silver was more expensive than gold in Egypt until around the fifteenth century BC:[34] the Egyptians are thought to have separated gold from silver by heating the metals with salt, and then reducing the silver chloride produced to the metal.[35]
The situation changed with the discovery of cupellation, a technique that allowed silver metal to be extracted from its ores. While slag heaps found in Asia Minor and on the islands of the Aegean Sea indicate that silver was being separated from lead as early as the 4th millennium BC,[36] and one of the earliest silver extraction centres in Europe was Sardinia in the early Chalcolithic period,[37] these techniques did not spread widely until later, when it spread throughout the region and beyond.[34] The origins of silver production in India, China, and Japan were almost certainly equally ancient, but are not well-documented due to their great age.[35]

When the Phoenicians first came to what is now Spain, they obtained so much silver that they could not fit it all on their ships, and as a result used silver to weight their anchors instead of lead.[34] By the time of the Greek and Roman civilizations, silver coins were a staple of the economy:[32] the Greeks were already extracting silver from galena by the 7th century BC,[34] and the rise of Athens was partly made possible by the nearby silver mines at Laurium, from which they extracted about 30 tonnes a year from 600 to 300 BC.[38] The stability of the Roman currency relied to a high degree on the supply of silver bullion, mostly from Spain, which Roman miners produced on a scale unparalleled before the discovery of the New World. Reaching a peak production of 200 tonnes per year, an estimated silver stock of 10000 tonnes circulated in the Roman economy in the middle of the second century AD, five to ten times larger than the combined amount of silver available to medieval Europe and the Abbasid Caliphate around AD 800.[39][40] The Romans also recorded the extraction of silver in central and northern Europe in the same time period. This production came to a nearly complete halt with the fall of the Roman Empire, not to resume until the time of Charlemagne: by then, tens of thousands of tonnes of silver had already been extracted.[35]
Central Europe became the centre of silver production during the Middle Ages, as the Mediterranean deposits exploited by the ancient civilisations had been exhausted. Silver mines were opened in Bohemia, Saxony, Erzgebirge, Alsace, the Lahn region, Siegerland, Silesia, Hungary, Norway, Steiermark, Salzburg, and the southern Black Forest. Most of these ores were quite rich in silver and could simply be separated by hand from the remaining rock and then smelted; some deposits of native silver were also encountered. Many of these mines were soon exhausted, but a few of them remained active until the Industrial Revolution, before which the world production of silver was around a meagre 50 tonnes per year.[35] In the Americas, high temperature silver-lead cupellation technology was developed by pre-Inca civilizations as early as AD 60–120; silver deposits in India, China, Japan, and pre-Columbian America continued to be mined during this time.[35][41]
With the discovery of America and the plundering of silver by the Spanish conquistadors, Central and South America became the dominant producers of silver until around the beginning of the 18th century, particularly Peru, Bolivia, Chile, and Argentina:[35] the last of these countries later took its name from that of the metal that composed so much of its mineral wealth.[38] The silver trade gave way to a global network of exchange. As one historian put it, silver "went round the world and made the world go round."[42] Much of this silver ended up in the hands of the Chinese. A Portuguese merchant in 1621 noted that silver "wanders throughout all the world... before flocking to China, where it remains as if at its natural center."[43] Still, much of it went to Spain, allowing Spanish rulers to pursue military and political ambitions in both Europe and the Americas. "New World mines," concluded several historians, "supported the Spanish empire."[44]
In the 19th century, primary production of silver moved to North America, particularly Canada, Mexico, and Nevada in the United States: some secondary production from lead and zinc ores also took place in Europe, and deposits in Siberia and the Russian Far East as well as in Australia were mined.[35] Poland emerged as an important producer during the 1970s after the discovery of copper deposits that were rich in silver, before the centre of production returned to the Americas the following decade. Today, Peru and Mexico are still among the primary silver producers, but the distribution of silver production around the world is quite balanced and about one-fifth of the silver supply comes from recycling instead of new production.[35]
-
Proto-Elamite kneeling bull holding a spouted vessel; 3100–2900 BC; 16.3 x 6.3 x 10.8 cm; Metropolitan Museum of Art (New York City)
-
Ancient Egyptian figurine of Horus as falcon god with an Egyptian crown; circa 500 BC; silver and electrum; height: 26.9 cm; Staatliche Sammlung für Ägyptische Kunst (Munich, Germany)
-
Ancient Greek tetradrachm; 315–308 BC; diameter: 2.7 cm; Metropolitan Museum of Art
-
Ancient Greek gilded bowl; 2nd–1st century BC; height: 7.6 cm, dimeter: 14.8 cm; Metropolitan Museum of Art
-
Roman plate; 1st–2nd century AD; height: 0.1 cm, diameter: 12.7 cm; Metropolitan Museum of Art
-
Roman bust of Serapis; 2nd century; 15.6 x 9.5 cm; Metropolitan Museum of Art
-
Auricular basin with scenes from the story of Diana and Actaeon; 1613; length: 50 cm, height: 6 cm, width: 40 cm; Rijksmuseum (Amsterdam, the Netherlands)
-
French Rococo tureen; 1749; height: 26.3 cm, width: 39 cm, depth: 24 cm; Metropolitan Museum of Art
-
French Rococo coffeepot; 1757; height: 29.5 cm; Metropolitan Museum of Art
-
French Neoclassical ewer; 1784–1785; height: 32.9 cm; Metropolitan Museum of Art
-
Neo-Rococo coffeepot; 1845; overall: 32 x 23.8 x 15.4 cm; Cleveland Museum of Art (Cleveland, Ohio, USA)
-
French Art Nouveau dessert spoons; circa 1890; Cooper Hewitt, Smithsonian Design Museum (New York City)
-
Art Nouveau jardinière; circa 1905–1910; height: 22 cm, width: 47 cm, depth: 22.5 cm; Cooper Hewitt, Smithsonian Design Museum
Symbolic role

Silver plays a certain role in mythology and has found various usage as a metaphor and in folklore. The Greek poet Hesiod's Works and Days (lines 109–201) lists different ages of man named after metals like gold, silver, bronze and iron to account for successive ages of humanity.[45] Ovid's Metamorphoses contains another retelling of the story, containing an illustration of silver's metaphorical use of signifying the second-best in a series, better than bronze but worse than gold:
{{{1}}}
In folklore, silver was commonly thought to have mystic powers: for example, a bullet cast from silver is often supposed in such folklore the only weapon that is effective against a werewolf, witch, or other monsters.[46][47][48] From this the idiom of a silver bullet developed into figuratively referring to any simple solution with very high effectiveness or almost miraculous results, as in the widely discussed software engineering paper No Silver Bullet.[49] Other powers attributed to silver include detection of poison and facilitation of passage into the mythical realm of fairies.[48]
Silver production has also inspired figurative language. Clear references to cupellation occur throughout the Old Testament of the Bible, such as in Jeremiah's rebuke to Judah: "The bellows are burned, the lead is consumed of the fire; the founder melteth in vain: for the wicked are not plucked away. Reprobate silver shall men call them, because the Lord hath rejected them." (Jeremiah 6:19–20) Jeremiah was also aware of sheet silver, exemplifying the malleability and ductility of the metal: "Silver spread into plates is brought from Tarshish, and gold from Uphaz, the work of the workman, and of the hands of the founder: blue and purple is their clothing: they are all the work of cunning men." (Jeremiah 10:9)[34]
Silver also has more negative cultural meanings: the idiom thirty pieces of silver, referring to a reward for betrayal, references the bribe Judas Iscariot is said in the New Testament to have taken from Jewish leaders in Jerusalem to turn Jesus of Nazareth over to soldiers of the high priest Caiaphas.[50] Ethically, silver also symbolizes greed and degradation of consciousness; this is the negative aspect, the perverting of its value.[51]
Occurrence and production

The abundance of silver in the Earth's crust is 0.08 parts per million, almost exactly the same as that of mercury. It mostly occurs in sulfide ores, especially acanthite and argentite, Ag2S. Argentite deposits sometimes also contain native silver when they occur in reducing environments, and when in contact with salt water they are converted to chlorargyrite (including horn silver), AgCl, which is prevalent in Chile and New South Wales.[52] Most other silver minerals are silver pnictides or chalcogenides; they are generally lustrous semiconductors. Most true silver deposits, as opposed to argentiferous deposits of other metals, came from Tertiary period vulcanism.[53]
The principal sources of silver are the ores of copper, copper-nickel, lead, and lead-zinc obtained from Peru, Bolivia, Mexico, China, Australia, Chile, Poland and Serbia.[36] Peru, Bolivia and Mexico have been mining silver since 1546, and are still major world producers. Top silver-producing mines are Cannington (Australia), Fresnillo (Mexico), San Cristóbal (Bolivia), Antamina (Peru), Rudna (Poland), and Penasquito (Mexico).[54] Top near-term mine development projects through 2015 are Pascua Lama (Chile), Navidad (Argentina), Jaunicipio (Mexico), Malku Khota (Bolivia),[55] and Hackett River (Canada).[54] In Central Asia, Tajikistan is known to have some of the largest silver deposits in the world.[56]
Silver is usually found in nature combined with other metals, or in minerals that contain silver compounds, generally in the form of sulfides such as galena (lead sulfide) or cerussite (lead carbonate). So the primary production of silver requires the smelting and then cupellation of argentiferous lead ores, a historically important process.[57] Lead melts at 327 °C, lead oxide at 888 °C and silver melts at 960 °C. To separate the silver, the alloy is melted again at the high temperature of 960 °C to 1000 °C in an oxidizing environment. The lead oxidises to lead monoxide, then known as litharge, which captures the oxygen from the other metals present. The liquid lead oxide is removed or absorbed by capillary action into the hearth linings.[58][59][60]
- Ag(s) + 2Pb(s) + O2(g) → 2PbO(absorbed) + Ag(l)
Today, silver metal is primarily produced instead as a secondary byproduct of electrolytic refining of copper, lead, and zinc, and by application of the Parkes process on lead bullion from ore that also contains silver.[61] In such processes, silver follows the non-ferrous metal in question through its concentration and smelting, and is later purified out. For example, in copper production, purified copper is electrolytically deposited on the cathode, while the less reactive precious metals such as silver and gold collect under the anode as the so-called "anode slime". This is then separated and purified of base metals by treatment with hot aerated dilute sulfuric acid and heating with lime or silica flux, before the silver is purified to over 99.9% purity via electrolysis in nitrate solution.[52]
Commercial-grade fine silver is at least 99.9% pure, and purities greater than 99.999% are available. In 2014, Mexico was the top producer of silver (5,000 tonnes or 18.7% of the world's total of 26,800 t), followed by China (4,060 t) and Peru (3,780 t).[61]
In marine environments
Silver concentration is low in seawater (pmol/L). Levels vary by depth and between water bodies. Dissolved silver concentrations range from 0.3 pmol/L in coastal surface waters to 22.8 pmol/L in pelagic deep waters.[62] Analyzing the presence and dynamics of silver in marine environments is difficult due to these particularly low concentrations and complex interactions in the environment.[63] Although a rare trace metal, concentrations are greatly impacted by fluvial, aeolian, atmospheric, and upwelling inputs, as well as anthropogenic inputs via discharge, waste disposal, and emissions from industrial companies.[64][65] Other internal processes such as decomposition of organic matter may be a source of dissolved silver in deeper waters, which feeds into some surface waters through upwelling and vertical mixing.[65]
In the Atlantic and Pacific, silver concentrations are minimal at the surface but rise in deeper waters.[66] Silver is taken up by plankton in the photic zone, remobilized with depth, and enriched in deep waters. Silver is transported from the Atlantic to the other oceanic water masses.[64] In North Pacific waters, silver is remobilized at a slower rate and increasingly enriched compared to deep Atlantic waters. Silver has increasing concentrations that follow the major oceanic conveyor belt that cycles water and nutrients from the North Atlantic to the South Atlantic to the North Pacific.[67]
There is not an extensive amount of data focused on how marine life is affected by silver despite the likely deleterious effects it could have on organisms through bioaccumulation, association with particulate matters, and sorption.[62] Not until about 1984 did scientists begin to understand the chemical characteristics of silver and the potential toxicity. In fact, mercury is the only other trace metal that surpasses the toxic effects of silver; however, the full extent of silver toxicity is not expected in oceanic conditions because of its ability to transfer into nonreactive biological compounds.[68]
In one study, the presence of excess ionic silver and silver nanoparticles caused bioaccumulation effects on zebrafish organs and altered the chemical pathways within their gills.[69] In addition, very early experimental studies demonstrated how the toxic effects of silver fluctuate with salinity and other parameters, as well as between life stages and different species such as finfish, molluscs, and crustaceans.[70] Another study found raised concentrations of silver in the muscles and liver of dolphins and whales, indicating pollution of this metal within recent decades. Silver is not an easy metal for an organism to eliminate and elevated concentrations can cause death.[71]
Monetary use

The earliest known coins were minted in the kingdom of Lydia in Asia Minor around 600 BC.[72] The coins of Lydia were made of electrum, which is a naturally occurring alloy of gold and silver, that was available within the territory of Lydia.[72] Since that time, silver standards, in which the standard economic unit of account is a fixed weight of silver, have been widespread throughout the world until the 20th century. Notable silver coins through the centuries include the Greek drachma,[73] the Roman denarius,[74] the Islamic dirham,[75] the karshapana from ancient India and rupee from the time of the Mughal Empire (grouped with copper and gold coins to create a trimetallic standard),[76] and the Spanish dollar.[77][78]
The ratio between the amount of silver used for coinage and that used for other purposes has fluctuated greatly over time; for example, in wartime, more silver tends to have been used for coinage to finance the war.[79]
Today, silver bullion has the ISO 4217 currency code XAG, one of only four precious metals to have one (the others being palladium, platinum, and gold).[80] Silver coins are produced from cast rods or ingots, rolled to the correct thickness, heat-treated, and then used to cut blanks from. These blanks are then milled and minted in a coining press; modern coining presses can produce 8000 silver coins per hour.[79]
Price
Silver prices are normally quoted in troy ounces. One troy ounce is equal to 31,1034768 gram. The London silver fix is published every working day at noon London time.[81] This price is determined by several major international banks and is used by London bullion market members for trading that day. Prices are most commonly shown as the United States dollar (USD), the Pound sterling (GBP), and the Euro (EUR).
Applications
Jewellery and silverware


The major use of silver besides coinage throughout most of history was in the manufacture of jewellery and other general-use items, and this continues to be a major use today. Examples include table silver for cutlery, for which silver is highly suited due to its antibacterial properties. Western concert flutes are usually plated with or made out of sterling silver;[83] in fact, most silverware is only silver-plated rather than made out of pure silver; the silver is normally put in place by electroplating. Silver-plated glass (as opposed to metal) is used for mirrors, vacuum flasks, and Christmas tree decorations.[84]
Because pure silver is very soft, most silver used for these purposes is alloyed with copper, with finenesses of 925/1000, 835/1000, and 800/1000 being common. One drawback is the easy tarnishing of silver in the presence of hydrogen sulfide and its derivatives. Including precious metals such as palladium, platinum, and gold gives resistance to tarnishing but is quite costly; base metals like zinc, cadmium, silicon, and germanium do not totally prevent corrosion and tend to affect the lustre and colour of the alloy. Electrolytically refined pure silver plating is effective at increasing resistance to tarnishing. The usual solutions for restoring the lustre of tarnished silver are dipping baths that reduce the silver sulfide surface to metallic silver, and cleaning off the layer of tarnish with a paste; the latter approach also has the welcome side effect of polishing the silver concurrently.[83] A simple chemical approach to removal of the sulfide tarnish is to bring silver items into contact with aluminium foil whilst immersed in water containing a conducting salt, such as sodium chloride.[kilde mangler]
Medicine
In medicine, silver is incorporated into wound dressings and used as an antibiotic coating in medical devices. Wound dressings containing silver sulfadiazine or silver nanomaterials are used to treat external infections. Silver is also used in some medical applications, such as urinary catheters (where tentative evidence indicates it reduces catheter-related urinary tract infections) and in endotracheal breathing tubes (where evidence suggests it reduces ventilator-associated pneumonia).[85][86] The silver ion is bioactive and in sufficient concentration readily kills bacteria in vitro. Silver ions interfere with enzymes in the bacteria that transport nutrients, form structures, and synthesise cell walls; these ions also bond with the bacteria's genetic material. Silver and silver nanoparticles are used as an antimicrobial in a variety of industrial, healthcare, and domestic application: for example, infusing clothing with nanosilver particles thus allows them to stay odourless for longer.[87][88] Bacteria can, however, develop resistance to the antimicrobial action of silver.[89] Silver compounds are taken up by the body like mercury compounds, but lack the toxicity of the latter. Silver and its alloys are used in cranial surgery to replace bone, and silver–tin–mercury amalgams are used in dentistry.[84] Silver diammine fluoride, the fluoride salt of a coordination complex with the formula [Ag(NH3)2]F, is a topical medicament (drug) used to treat and prevent dental caries (cavities) and relieve dentinal hypersensitivity.[90]
Electronics
Silver is very important in electronics for conductors and electrodes on account of its high electrical conductivity even when tarnished. Bulk silver and silver foils were used to make vacuum tubes, and continue to be used today in the manufacture of semiconductor devices, circuits, and their components. For example, silver is used in high quality connectors for RF, VHF, and higher frequencies, particularly in tuned circuits such as cavity filters where conductors cannot be scaled by more than 6%. Printed circuits and RFID antennas are made with silver paints,[36][91] Powdered silver and its alloys are used in paste preparations for conductor layers and electrodes, ceramic capacitors, and other ceramic components.[92]
Brazing alloys
Silver-containing brazing alloys are used for brazing metallic materials, mostly cobalt, nickel, and copper-based alloys, tool steels, and precious metals. The basic components are silver and copper, with other elements selected according to the specific application desired: examples include zinc, tin, cadmium, palladium, manganese, and phosphorus. Silver provides increased workability and corrosion resistance during usage.[93]
Chemical equipment
Silver is useful in the manufacture of chemical equipment on account of its low chemical reactivity, high thermal conductivity, and being easily workable. Silver crucibles (alloyed with 0.15% nickel to avoid recrystallisation of the metal at red heat) are used for carrying out alkaline fusion. Copper and silver are also used when doing chemistry with fluorine. Equipment made to work at high temperatures is often silver-plated. Silver and its alloys with gold are used as wire or ring seals for oxygen compressors and vacuum equipment.[94]
Catalysis
Silver metal is a good catalyst for oxidation reactions; in fact it is somewhat too good for most purposes, as finely divided silver tends to result in complete oxidation of organic substances to carbon dioxide and water, and hence coarser-grained silver tends to be used instead. For instance, 15% silver supported on α-Al2O3 or silicates is a catalyst for the oxidation of ethylene to ethylene oxide at 230–270 °C. Dehydrogenation of methanol to formaldehyde is conducted at 600–720 °C over silver gauze or crystals as the catalyst, as is dehydrogenation of isopropanol to acetone. In the gas phase, glycol yields glyoxal and ethanol yields acetaldehyde, while organic amines are dehydrated to nitriles.[94]
Photography
The photosensitivity of the silver halides allowed for their use in traditional photography, although digital photography, which does not use silver, is now dominant. The photosensitive emulsion used in black-and-white photography is a suspension of silver halide crystals in gelatin, possibly mixed in with some noble metal compounds for improved photosensitivity, developing, and tuning. Colour photography requires the addition of special dye components and sensitisers, so that the initial black-and-white silver image couples with a different dye component. The original silver images are bleached off and the silver is then recovered and recycled. Silver nitrate is the starting material in all cases.[95]
The use of silver nitrate and silver halides in photography has rapidly declined with the advent of digital technology. From the peak global demand for photographic silver in 1999 (267,000,000 troy ounces or 8304.6 metric tonnes) the market contracted almost 70% by 2013.[96]
Nanoparticles
Nanosilver particles, between 10 and 100 nanometres in size, are used in many applications. They are used in conductive inks for printed electronics, and have a much lower melting point than larger silver particles of micrometre size. They are also used medicinally in antibacterials and antifungals in much the same way as larger silver particles.[88] In addition, according to the European Union Observatory for Nanomaterials (EUON), silver nanoparticles are used both in pigments, as well as cosmetics.[97][98]
Miscellanea

Pure silver metal is used as a food colouring. It has the E174 designation and is approved in the European Union.[99] Traditional Pakistani and Indian dishes sometimes include decorative silver foil known as vark,[100] and in various other cultures, silver dragée are used to decorate cakes, cookies, and other dessert items.[101]
Photochromic lenses include silver halides, so that ultraviolet light in natural daylight liberates metallic silver, darkening the lenses. The silver halides are reformed in lower light intensities. Colourless silver chloride films are used in radiation detectors. Zeolite sieves incorporating Ag+ ions are used to desalinate seawater during rescues, using silver ions to precipitate chloride as silver chloride. Silver is also used for its antibacterial properties for water sanitisation, but the application of this is limited by limits on silver consumption. Colloidal silver is similarly used to disinfect closed swimming pools; while it has the advantage of not giving off a smell like hypochlorite treatments do, colloidal silver is not effective enough for more contaminated open swimming pools. Small silver iodide crystals are used in cloud seeding to cause rain.[88]
Precautions
Skabelon:Chembox Silver compounds have low toxicity compared to those of most other heavy metals, as they are poorly absorbed by the human body when digested, and that which does get absorbed is rapidly converted to insoluble silver compounds or complexed by metallothionein. However, silver fluoride and silver nitrate are caustic and can cause tissue damage, resulting in gastroenteritis, diarrhoea, falling blood pressure, cramps, paralysis, and respiratory arrest. Animals repeatedly dosed with silver salts have been observed to experience anaemia, slowed growth, necrosis of the liver, and fatty degeneration of the liver and kidneys; rats implanted with silver foil or injected with colloidal silver have been observed to develop localised tumours. Parenterally admistered colloidal silver causes acute silver poisoning.[102] Some waterborne species are particularly sensitive to silver salts and those of the other precious metals; in most situations, however, silver does not pose serious environmental hazards.[102]
In large doses, silver and compounds containing it can be absorbed into the circulatory system and become deposited in various body tissues, leading to argyria, which results in a blue-grayish pigmentation of the skin, eyes, and mucous membranes. Argyria is rare, and so far as is known, does not otherwise harm a person's health, though it is disfiguring and usually permanent. Mild forms of argyria are sometimes mistaken for cyanosis.[102][36]
Metallic silver, like copper, is an antibacterial agent, which was known to the ancients and first scientifically investigated and named the oligodynamic effect by Carl Nägeli. Silver ions damage the metabolism of bacteria even at such low concentrations as 0.01–0.1 milligrams per litre; metallic silver has a similar effect due to the formation of silver oxide. This effect is lost in the presence of sulfur due to the extreme insolubility of silver sulfide.[102]
Some silver compounds are very explosive, such as the nitrogen compounds silver azide, silver amide, and silver fulminate, as well as silver acetylide, silver oxalate, and silver(II) oxide. They can explode on heating, force, drying, illumination, or sometimes spontaneously. To avoid the formation of such compounds, ammonia and acetylene should be kept away from silver equipment. Salts of silver with strongly oxidising acids such as silver chlorate and silver nitrate can explode on contact with materials that can be readily oxidised, such as organic compounds, sulfur and soot.[102]
See also
- Silver coin
- Silver medal
- Free silver
- List of countries by silver production
- List of silver compounds
- Silver as an investment
- Silverpoint drawing
References
- ^ a b Greenwood and Earnshaw, p. 1179
- ^ a b Fodnotefejl: Ugyldigt
<ref>-tag; ingen tekst er angivet for referencer med navnetGreenwood1177 - ^ a b c d e Greenwood and Earnshaw, p. 1180
- ^ Greenwood and Earnshaw, p. 1176
- ^ Lidin RA 1996, Inorganic substances handbook, Begell House, New York, ISBN 1-56700-065-7. p. 5
- ^ Goodwin F, Guruswamy S, Kainer KU, Kammer C, Knabl W, Koethe A, Leichtfreid G, Schlamp G, Stickler R & Warlimont H 2005, 'Noble metals and noble metal alloys', in Springer Handbook of Condensed Matter and Materials Data, W Martienssen & H Warlimont (eds), Springer, Berlin, pp. 329–406, ISBN 3-540-44376-2. p. 341
- ^ "Silver Artifacts" in Corrosion – Artifacts. NACE Resource Center
- ^ Bjelkhagen, Hans I. (1995). Silver-halide recording materials: for holography and their processing. Springer. s. 156–66. ISBN 978-3-540-58619-7.
- ^ Riedel, Sebastian; Kaupp, Martin (2009). "The highest oxidation states of the transition metal elements". Coordination Chemistry Reviews. 253 (5-6): 606-24. doi:10.1016/j.ccr.2008.07.014.
- ^ a b Greenwood and Earnshaw, p. 1188
- ^ Greenwood and Earnshaw, p. 903
- ^ a b c Greenwood and Earnshaw, pp. 1181–82
- ^ a b c d e Greenwood and Earnshaw, pp. 1183–85
- ^ a b Fodnotefejl: Ugyldigt
<ref>-tag; ingen tekst er angivet for referencer med navnetIUPAC - ^ a b Greenwood and Earnshaw, pp. 1185–87
- ^ "Definition of Lunar Caustic". dictionary.die.net. Arkiveret fra originalen den 31 januar 2012.
{{cite web}}: CS1-vedligeholdelse: BOT: original-url status ukendt (link) CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Skabelon:OrgSynth
- ^ a b Skabelon:OrgSynth
- ^ Andreas Brumby et al. "Silver, Silver Compounds, and Silver Alloys" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2008.
- ^ Meyer, Rudolf; Köhler, Josef & Homburg, Axel (2007). Explosives. Wiley–VCH. s. 284. ISBN 978-3-527-31656-4.
- ^ Greenwood and Earnshaw, p. 1189
- ^ Greenwood and Earnshaw, pp. 1195–96
- ^ Greenwood and Earnshaw, pp. 1199–200
- ^ Miller, W.T.; Burnard, R.J. (1968). "Perfluoroalkylsilver compounds". J. Am. Chem. Soc. 90 (26): 7367-68. doi:10.1021/ja01028a047.
- ^ Holliday, A.; Pendlebury, R.E. (1967). "Vinyllead compounds I. Cleavage of vinyl groups from tetravinyllead". J. Organomet. Chem. 7 (2): 281-84. doi:10.1016/S0022-328X(00)91078-7.
- ^ Wang, Harrison M.J.; Lin, Ivan J.B. (1998). "Facile Synthesis of Silver(I)−Carbene Complexes. Useful Carbene Transfer Agents". Organometallics. 17 (5): 972-75. doi:10.1021/om9709704.
- ^ a b Ullmann, pp. 54–61
- ^ Kroonen, Guus (2013). Etymological Dictionary of Proto-Germanic (engelsk). Brill. s. 436. ISBN 978-90-04-18340-7.
- ^ a b Mallory, James P.; Adams, Douglas Q. (2006). The Oxford Introduction to Proto-Indo-European and the Proto-Indo-European World (engelsk). Oxford University Press. s. 241-242. ISBN 978-0-19-928791-8.
- ^ Boutkan, Dirk; Kossmann, Maarten (2001). "On the Etymology of "Silver"". NOWELE. North-Western European Language Evolution (engelsk). 38 (1): 3-15. doi:10.1075/nowele.38.01bou. ISSN 0108-8416.
- ^ Weeks, p. 4
- ^ a b c Greenwood and Earnshaw, pp. 1173–74
- ^ Readon, Arthur C. (2011). Metallurgy for the Non-Metallurgist. ASM International. s. 73-84. ISBN 978-1-61503-821-3.
- ^ a b c d e Weeks, pp. 14–19
- ^ a b c d e f g h Ullmann, pp. 16–19
- ^ a b c d Fodnotefejl: Ugyldigt
<ref>-tag; ingen tekst er angivet for referencer med navnetCRC - ^ Maria Grazia Melis. "Silver in Neolithic and Eneolithic Sardinia, in H. Meller/R. Risch/E. Pernicka (eds.), Metalle der Macht – Frühes Gold und Silber. 6. Mitteldeutscher Archäologentag vom 17. bis 19. Oktober 2013 in Halle (Saale), Tagungen des Landesmuseums für".
{{cite journal}}: Cite journal kræver|journal=(hjælp) - ^ a b Emsley, John (2011). Nature's building blocks: an A-Z guide to the elements. Oxford University Press. s. 492-98. ISBN 978-0-19-960563-7.
- ^ Patterson, C.C. (1972). "Silver Stocks and Losses in Ancient and Medieval Times". The Economic History Review. 25 (2): 205235 (216, table 2, 228, table 6). doi:10.1111/j.1468-0289.1972.tb02173.x.
- ^ de Callataÿ, François (2005). "The Greco-Roman Economy in the Super Long-Run: Lead, Copper, and Shipwrecks". Journal of Roman Archaeology. 18: 361–72 [365ff]. doi:10.1017/s104775940000742x.
- ^ Carol A. Schultze; Charles Stanish; David A. Scott; Thilo Rehren; Scott Kuehner; James K. Feathers (2009). "Direct evidence of 1,900 years of indigenous silver production in the Lake Titicaca Basin of Southern Peru". Proceedings of the National Academy of Sciences of the United States of America. 106 (41): 17280-83. Bibcode:2009PNAS..10617280S. doi:10.1073/pnas.0907733106. PMC 2754926. PMID 19805127.
- ^ Frank, Andre Gunder (1998). ReOrient: Global Economy in the Asian Age. Berkeley: University of California Press. s. 131.
- ^ von Glahn, Richard (1996). "Myth and Reality of China's Seventeenth Century Monetary Crisis". Journal of Economic History. 2: 132.
- ^ Flynn, Dennis O.; Giraldez, Arturo (1995). "Born with a "Silver Spoon"". Journal of World History. 2: 210.
- ^ Joseph Eddy Fontenrose: Work, Justice, and Hesiod's Five Ages. In: Classical Philology. V. 69, Nr. 1, 1974, p. 1–16.
- ^ Jackson, Robert (1995). Witchcraft and the Occult. Devizes, Quintet Publishing. s. 25. ISBN 978-1-85348-888-7.
- ^ Стойкова, Стефана. "Дельо хайдутин". Българска народна поезия и проза в седем тома (bulgarsk). Vol. Т. III. Хайдушки и исторически песни. Варна: ЕИ "LiterNet". ISBN 978-954-304-232-6.
- ^ a b St. Clair, Kassia (2016). The Secret Lives of Colour. London: John Murray. s. 49. ISBN 9781473630819. OCLC 936144129.
- ^ Brooks, Frederick. P., Jr. (1987). "No Silver Bullet – Essence and Accident in Software Engineering" (PDF). Computer. 20 (4): 10-19. CiteSeerX 10.1.1.117.315. doi:10.1109/MC.1987.1663532. S2CID 372277.
- ^ Skabelon:Bibleverse
- ^ Chevalier, Jean; Gheerbrant, Alain (2009). Dicționar de Simboluri. Mituri, Vise, Obiceiuri, Gesturi, Forme, Figuri, Culori, Numere [Dictionary of Symbols. Myths, Dreams, Habits, Gestures, Shapes, Figures, Colors, Numbers] (rumænsk). Polirom. 105. ISBN 978-973-46-1286-4.
- ^ a b Greenwood and Earnshaw, pp. 1174–67
- ^ Ullmann, pp. 21–22
- ^ a b CPM Group (2011). CPM Silver Yearbook. New York: Euromoney Books. s. 68. ISBN 978-0-9826741-4-7.
- ^ "Preliminary Economic Assessment Technical Report 43-101" (PDF). South American Silver Corp. Arkiveret fra originalen (PDF) 19 januar 2012.
{{cite web}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ "Why Are Kyrgyzstan and Tajikistan So Split on Foreign Mining?". EurasiaNet.org. 7 august 2013. Hentet 19 august 2013.
{{cite web}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Kassianidou, V. 2003. Early Extraction of Silver from Complex Polymetallic Ores, in Craddock, P.T. and Lang, J (eds) Mining and Metal production through the Ages. London, British Museum Press: 198–206
- ^ Craddock, P.T. (1995). Early metal mining and production. Edinburgh: Edinburgh University Press. p. 223
- ^ Bayley, J., Crossley, D. and Ponting, M. (eds). 2008. "Metals and Metalworking. A research framework for archaeometallurgy". Historical Metallurgy Society 6.
- ^ Pernicka, E., Rehren, Th., Schmitt-Strecker, S. 1998. Late Uruk silver production by cupellation at Habuba Kabira, Syria in Metallurgica Antiqua : in honour of Hans-Gert Bachmann and Robert Maddin by Bachmann, H.G, Maddin, Robert, Rehren, Thilo, Hauptmann, Andreas, Muhly, James David, Deutsches Bergbau-Museum: 123–34.
- ^ a b Hilliard, Henry E. "Silver". USGS.
- ^ a b Barriada, Jose L.; Tappin, Alan D.; Evans, E. Hywel; Achterberg, Eric P. (2007). "Dissolved silver measurements in seawater". TrAC Trends in Analytical Chemistry. 26 (8): 809-817. doi:10.1016/j.trac.2007.06.004. ISSN 0165-9936.
- ^ Fischer, Lisa; Smith, Geoffrey; Hann, Stephan; Bruland, Kenneth W. (2018). "Ultra-trace analysis of silver and platinum in seawater by ICP-SFMS after off-line matrix separation and pre-concentration". Marine Chemistry. 199: 44-52. doi:10.1016/j.marchem.2018.01.006. ISSN 0304-4203.
- ^ a b Ndung’u, K.; Thomas, M.A.; Flegal, A.R. (2001). "Silver in the western equatorial and South Atlantic Ocean". Deep Sea Research Part II: Topical Studies in Oceanography. 48 (13): 2933-2945. doi:10.1016/S0967-0645(01)00025-X. ISSN 0967-0645.
- ^ a b Zhang, Yan; Amakawa, Hiroshi; Nozaki, Yoshiyuki (2001). "Oceanic profiles of dissolved silver: precise measurements in the basins of western North Pacific, Sea of Okhotsk, and the Japan Sea". Marine Chemistry. 75 (1-2): 151-163. doi:10.1016/S0304-4203(01)00035-4. ISSN 0304-4203.
- ^ Flegal, A.R.; Sañudo-Wilhelmy, S.A.; Scelfo, G.M. (1995). "Silver in the Eastern Atlantic Ocean". Marine Chemistry. 49 (4): 315-320. doi:10.1016/0304-4203(95)00021-I. ISSN 0304-4203.
- ^ Ranville, Mara A.; Flegal, A. Russell (2005). "Silver in the North Pacific Ocean". Geochemistry, Geophysics, Geosystems. 6 (3): n/a–n/a. doi:10.1029/2004GC000770. ISSN 1525-2027.
- ^ Ratte, Hans Toni (1999). "Bioaccumulation and toxicity of silver compounds: A review". Environmental Toxicology and Chemistry. 18 (1): 89-108. doi:10.1002/etc.5620180112. ISSN 0730-7268.
- ^ Lacave, José María; Vicario-Parés, Unai; Bilbao, Eider; Gilliland, Douglas; Mura, Francesco; Dini, Luciana; Cajaraville, Miren P.; Orbea, Amaia (2018). "Waterborne exposure of adult zebrafish to silver nanoparticles and to ionic silver results in differential silver accumulation and effects at cellular and molecular levels". Science of The Total Environment. 642: 1209-1220. doi:10.1016/j.scitotenv.2018.06.128. ISSN 0048-9697.
- ^ Calabrese, A., Thurberg, F.P., Gould, E. (1977). Effects of Cadmium, Mercury, and Silver on Marine Animals. Marine Fisheries Review, 39(4):5-11. https://fliphtml5.com/hzci/lbsc/basic
- ^ Chen, Meng-Hsien; Zhuang, Ming-Feng; Chou, Lien-Siang; Liu, Jean-Yi; Shih, Chieh-Chih; Chen, Chiee-Young (2017). "Tissue concentrations of four Taiwanese toothed cetaceans indicating the silver and cadmium pollution in the western Pacific Ocean". Marine Pollution Bulletin. 124 (2): 993-1000. doi:10.1016/j.marpolbul.2017.03.028. ISSN 0025-326X.
- ^ a b "The origins of coinage". britishmuseum.org. Hentet september 21, 2015.
{{cite web}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ "Tetradrachm". Merriam-Webster. Hentet 2008-01-20.
- ^ Crawford, Michael H. (1974). Roman Republican Coinage, Cambridge University Press, 2 Volumes. ISBN 0-521-07492-4
- ^ Oxford English Dictionary, 1st edition, s.v. 'dirhem'
- ^ etymonline.com (september 20, 2008). "Etymology of rupee". Hentet 2008-09-20.
{{cite web}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Ray Woodcock (1 maj 2009). Globalization from Genesis to Geneva: A Confluence of Humanity. Trafford Publishing. s. 104-05. ISBN 978-1-4251-8853-5. Hentet 13 august 2013.
{{cite book}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Thomas J. Osborne (2012). Pacific Eldorado: A History of Greater California. John Wiley & Sons. s. 31. ISBN 978-1-118-29217-4. Hentet 13 august 2013.
{{cite book}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ a b Ullmann, pp. 63–65
- ^ "Current currency & funds code list – ISO Currency". SNV. Hentet 2020-03-29.
- ^ "LBMA Silver Price". LBMA. Hentet 2020-03-29.
- ^ Marcin Latka. "Silver sarcophagus of Saint Stanislaus". artinpl. Hentet 3 august 2019.
{{cite web}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ a b Ullmann, pp. 65–67
- ^ a b Ullmann, pp. 67–71
- ^ Beattie, M.; Taylor, J. (2011). "Silver alloy vs. Uncoated urinary catheters: A systematic review of the literature". Journal of Clinical Nursing. 20 (15-16): 2098-108. doi:10.1111/j.1365-2702.2010.03561.x. PMID 21418360.
- ^ Bouadma, L.; Wolff, M.; Lucet, J.C. (august 2012). "Ventilator-associated pneumonia and its prevention". Current Opinion in Infectious Diseases. 25 (4): 395-404. doi:10.1097/QCO.0b013e328355a835. PMID 22744316. S2CID 41051853.
{{cite journal}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Maillard, Jean-Yves; Hartemann, Philippe (2012). "Silver as an antimicrobial: Facts and gaps in knowledge". Critical Reviews in Microbiology. 39 (4): 373-83. doi:10.3109/1040841X.2012.713323. PMID 22928774. S2CID 27527124.
- ^ a b c Ullmann, pp. 83–84
- ^
Panáček, Aleš; Kvítek, Libor; Smékalová, Monika; Večeřová, Renata; Kolář, Milan; Röderová, Magdalena; Dyčka, Filip; Šebela, Marek; Prucek, Robert; Tomanec, Ondřej; Zbořil, Radek (januar 2018). "Bacterial resistance to silver nanoparticles and how to overcome it". Nature Nanotechnology. 13 (1): 65-71. Bibcode:2018NatNa..13...65P. doi:10.1038/s41565-017-0013-y. PMID 29203912. S2CID 26783560.
{{cite journal}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Rosenblatt, A.; Stamford, T.C.M.; Niederman, R. (2009). "Silver diamine fluoride: a caries "silver-fluoride bullet"". Journal of Dental Research. 88 (2): 116-25. doi:10.1177/0022034508329406. PMID 19278981. S2CID 30730306.
- ^ Nikitin, Pavel V.; Lam, Sander & Rao, K.V.S. (2005). "Low Cost Silver Ink RFID Tag Antennas" (PDF). 2005 IEEE Antennas and Propagation Society International Symposium. Vol. 2B. s. 353. doi:10.1109/APS.2005.1552015. ISBN 978-0-7803-8883-3. S2CID 695256. Arkiveret fra originalen den 21 marts 2016.
{{cite book}}: CS1-vedligeholdelse: BOT: original-url status ukendt (link) CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Ullmann, pp. 71–78
- ^ Ullmann, pp. 78–81
- ^ a b Ullmann, pp. 81–82
- ^ Ullmann, p. 82
- ^ "A Big Source of Silver Bullion Demand Has Disappeared". BullionVault. Hentet 2014-07-20.
- ^ "European Union Observatory for Nanomaterials pigments inventory".
- ^ "European Union Observatory for Nanomaterials catalogue of nano cosmetics ingredients".
- ^ Martínez-Abad, A.; Ocio, M.J.; Lagarón, J.M.; Sánchez, G. (2013). "Evaluation of silver-infused polylactide films for inactivation of Salmonella and feline calicivirus in vitro and on fresh-cut vegetables". International Journal of Food Microbiology. 162 (1): 89-94. doi:10.1016/j.ijfoodmicro.2012.12.024. PMID 23376782.
- ^ Sarvate, Sarita (4 april 2005). "Silver Coating". India Currents. Arkiveret fra originalen den 14 februar 2009. Hentet 5 juli 2009.
{{cite news}}: CS1-vedligeholdelse: BOT: original-url status ukendt (link) CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ Meisler, Andy (18 december 2005). "A Tempest on a Tea Cart". Los Angeles Times.
{{cite news}}: CS1-vedligeholdelse: Dato automatisk oversat (link) - ^ a b c d e Ullmann, pp. 88–91
Sources used above
- Skabelon:Greenwood&Earnshaw2nd
- Weeks, Mary Elvira; Leichester, Henry M. (1968). Discovery of the Elements. Easton, PA: Journal of Chemical Education. ISBN 978-0-7661-3872-8. LCCN 68-15217.
- "Silver, Silver Compounds, and Silver Alloys". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a24_107.pub2. ISBN 978-3527306732.
Further reading
- William L. Silber, The Story of Silver: How the White Metal Shaped America and the Modern World. Princeton, NJ: Princeton University Press, 2019.
External links
| | Søsterprojekter med yderligere information: |
- Silver at The Periodic Table of Videos (University of Nottingham)
- Society of American Silversmiths
- The Silver Institute A silver industry website
- A collection of silver items Samples of silver
- Transport, Fate and Effects of Silver in the Environment
- CDC – NIOSH Pocket Guide to Chemical Hazards – Silver
- Picture in the Element collection from Heinrich Pniok















