Influenza
 Ikke at forveksle med Influencer.
Ikke at forveksle med Influencer.
| Influenza Klassifikation | |
|---|---|
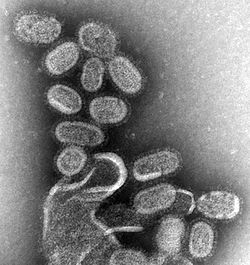 Elektronmikroskopi af bestemte influenzavironer, forstørret cirka 100.000 gange op. | |
| Information | |
| Navn | Influenza |
| Medicinsk fagområde |
lungemedicin, akutmedicin, almen medicin, infektionsmedicin |
| SKS | DJ10.0 |
| ICD-10 | J10.0 |
| ICD-9 |
487 |
| OMIM |
614680 |
| DiseasesDB |
6791 |
| MedlinePlus |
000080 |
| ICD-9-CM |
487, 487.8 |
| Patientplus |
influenza |
| MeSH |
D007251 |
|
Information med symbolet | |
Influenza er en infektionssygdom i fugle og pattedyr forårsaget af RNA-vira fra familien Orthomyxoviridae (influenzavira).[1] Navnet influenza kommer fra det italienske "influenza" som betyder "indflydelse" (latin: "influentia"). Hos mennesker er de mest udbredte symptomer på sygdommen forkølelse og feber, svælgkatar, muskelømhed, voldsom hovedpine, hoste, træthed og generelt fysisk ubehag.[2] I mere alvorlige tilfælde kan influenza føre til lungebetændelse, som kan være dødelig specielt hos små børn og gamle mennesker. Selvom den kan forveksles med almindelig forkølelse er influenza en alvorligere sygdom og skyldes en anden type af virussen.[3] Influenza kan føre til kvalme og opkast, specielt hos børn,[2] men disse symptomer er mere karakteristiske for den ikke-relaterede gastroenteritis, som nogle gange kaldes "maveinfluenza" eller "24-timers influenza".[4][5]
Influenza spreder sig typisk fra smittede pattedyr gennem luften ved hoste eller nys, som skaber aerosoler indeholdende virussen, og fra smittede fugle via deres afføring. Influenza kan også overføres via spyt, slim, afføring og blod. Infektioner sker også gennem kontakt med disse kropsvæsker eller med smitteoverflader. Influenzavira kan forblive smitsomme i omkring en uge ved legemstemperatur, over 30 dage ved 0 °C og i meget længere perioder ved lavere temperaturer.[6][7] De fleste influenzastrenge kan let inaktiveres ved desinfektion.[8][9][10]
Influenza spreder sig Jorden rundt i sæsonepidemier og resulterer i tusinder af døde og millioner i pandemiske år. Tre influenzapandemier dræbte i det 20. århundrede millioner af mennesker, og hver af disse pandemier skyldtes fremkomsten af en ny streng af virussen i mennesker. Sygdommen hed under den første af de tre pandemier den Spanske Syge som rasede i 1918. Ofte kommer disse nye strenge fra spredningen af en eksisterende influenzavirus til mennesker fra en anden dyreart. En dødelig streng af fugleinfluenza kaldet H5N1 har vist sig at være den største risiko for en ny influenzapandemi siden den krævede sine første menneskeofre i Asien i 1990'erne. Virussen har dog endnu ikke muteret til en form som spredes nemt blandt mennesker.[11]
Vaccinationer mod influenza gives ofte til mennesker i udviklede lande som har en vis sandsynlighed for at blive ramt af sygdommen,[12] samt til landbrugsfjerkræ.[13] Den mest udbredte menneskevaccine er influenzavaccinen som indeholder renset og inaktiveret materiale fra tre virale strenge. Denne vaccine omfatter typisk materiale fra to influenzavirus A-serotyper og en influenzavirus B-art.[14] En vaccine som blev formuleret til et år kan være ubrugelig det næste år, da influenzavirussen hurtigt ændrer sig, og andre strenge bliver dominerende. Antiviral medicin kan bruges til at behandle influenza, og neuraminidase-hæmmere er specielt effektive.
Symptomer[redigér | rediger kildetekst]
| Symptom: | sensitivitet | specificitet |
|---|---|---|
| Feber | 68–86% | 25–73% |
| Hoste | 84–98% | 7–29% |
| Nasal obstruktion | 68–91% | 19–41% |
|
| ||

Cirka 33% med influenza oplever ingen symptomer.[17]
Almindeligvis opstår influenzasymptomer pludseligt en til to dage efter infektionen. Oftest er de begyndende symptomer kulderystelser eller kuldefornemmelser, men feber er også almindeligt med kropstemperaturer mellem 38-39 °C.[18] Mange vil være så syge at de må blive i sengen i flere dage med ubehag og kropssmerter, som oftest er værst i ryggen og benene.[2] Influenzasymptomer inkluderer[19]:
- Feber og udtalt kuldefølelse lige fra dirren til rysten, høj feber, men kan dog variere
- Hoste
- Ondt i halsen, synke besvær
- Nasal obstruktion ("Snottet")
- Næseblod, sker kun i sjældne tilfælde med influenza eller forkølelse[20]
- Muskelømhed, ømhed, især i led, knogler og tænder
- Muskelsmerter og smerter i brystet
- Udmattelse, træthed, søvnbesvær og søvnløshed
- Forkølelse, evt. opkastning og diarré
- Kvalme
- Svimmelhed
- Svælgkatar
- Svækkelse
- Hovedpine
- Ondt i maven, mavepine
- Irritabilitet, våde øjne, synes besvær og ondt i øjnene
- Øjenbetændelse[21]
- Ondt i ørerne, ørepine
- Vejrtrækningsproblemer i meget sjældne tilfælde og influenza kan også udvikle sig til lungebetændelse og men influenza angriber normalt også lungerne[22][23][24][22][25][26][27][28]
- Kropsvarme, kroppen kan blive meget varm at blæren begynder at gøre meget ondt og at ens tis bliver virkelig varmt, som skoldhed vand, men kan dog variere og det samme symptomer ses også ved en almindelig blærebetændelse eller lignende
- Nedsat appetit
- Røde øjne, hud (især ansigt), mund, hals og næse
- I børn mave-tarm (gastrointestinale) symptomer, som diarre, opkastninger og smerter i bugen (abdominale smerter),[29][30] (ses ofte mere udtalte i børn med influenza B)[31]
Det kan være svært at skelne en almindelig forkølelse og en influenzainfektion i de begyndende stadier,[3] men influenza kan genkendes på den høje feber med pludseligt indsættende kropslig svækkelse. Diarre er normalt ikke et symptom blandt voksne[15] selvom det før har været dokumenteret ved H5N1 ("fugleinfluenza") infektion,[32] og kan være et symptom blandt børn.[29] De mest bekræftende symptomer på influenza er opgivet i tabellen til højre.[15]
Ved influenza kan der være risiko for sekundære komplikationer i form af pneumoni (lungebetændelse) enten skabt direkte af virus eller en bakterieinfektion.[33][34] Det mest karakteristiske symptom er vejrtrækningsproblemer. Dertil ses det at hvis et barn (eller antagelig en voksen) ser ud til at få det bedre, og oplever tilbagefald med høj feber, er dette et faresignal på bakteriæl pneumoni.[35][36][37][38][39]
Virologi[redigér | rediger kildetekst]
Virustyper[redigér | rediger kildetekst]

Influenzavira er RNAvira tilhørende Orthomyxoviridae-familien[40] og udgør herindenfor 4 slægter[41][42][43]:


- Influenzavirus A
- Influenzavirus B
- Influenzavirus C
- Influenzavirus D[44][45][46][47][48][49][45][50][51]
Disse vira er kun fjernt relateret til human parainfluenzavirus, som er RNA vira tilhørende paramyxovirusfamilien, der er en almindelig årsag til respiratoriske infektioner i børn som strubehoste (krup),[52] men kan ligeledes forårsage influenzalignende symptomer blandt voksne.[53]
Influenzavirus A[redigér | rediger kildetekst]

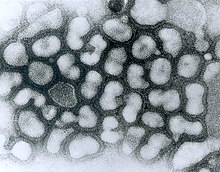
Dette virusmedlem har en virusart: Influenza A[54][55][56]. Dennes naturlige vært er vandfugle. Af og til overføres virus til andre arter, og kan derved forårsage voldsomme udbrud blandt husholdte fjerkræ eller humane influenzapandemier.[57] Type A virus er den mest virulente humane patogen blandt de tre influenzamedlemmer og medfører ligeså mere alvorlige sygdomme. Influenza virus A kan underinddeles i forskellige serotyper ud fra antistofresponset mod disse vira.[58] Serotyperne som er blevet dokumenteret i mennesker ordnet efter kendte humane pandemier er:
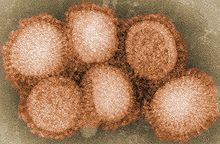
- H1N1: Den Spanske Syge i 1918, Fugleinfluenzaen i 2006, og Svineinfluenzaen i 2009 og Svineinfluenzaen igen i 2012[59][60][61]
- H1N2, endemisk i mennesker, svin og fugle
- H2N2: Den Asiatiske influenza i 1957
- H2N3: Fugleinfluenzaen i 2006
- H3N1, endemisk i mennesker og svin
- H3N2: Hong Kong influenzaen i 1968, og Den Russiske influenza i 1977 og H3N2, endemisk i mennesker i 1997, Fujian influenza i 2002 og Fugleinfluenzaen i 2018
- H3N8: Fugleinfluenzaen i 1889–1890, 1898–1900, 1963, 1964, 1965, 2011 og igen i 2022
- H5N1: Fugleinfluenzaen i 1997 og igen i 2003, 2004, 2005, 2011, 2016, 2017, 2020, 2021 og 2022[62]
- H5N8: Fugleinfluenzaen i 2016-2017, 2020, 2021 og 2022[63]
- H7N1: Fugleinfluenzaen i 1972 og igen i 1999
- H7N2: Fugleinfluenzaen i 1918, 1957, 1968, 2002, 2003, 2007, 2014 og igen i 2016
- H7N3: Fugleinfluenzaen i 1963, 1979, 2004, 2005, 2006, 2007 og igen i 2012
- H7N4: Fugleinfluenzaen i 2021
- H7N5: Fugleinfluenzaen i 2014
- H7N7, som har et usædvanligt zoonotisk potentiale, Fugleinfluenzaen i 2003, 2006, 2008, 2009, 2013, 2015 og igen i 2020[64][65]
- H7N9: Fugleinfluenzaen i 2013, 2017 og igen i 2021
- H9N2: Fugleinfluenzaen i 1966, 1999 og igen i 2003
- H5: Fugleinfluenzaen i 2019
- H7: Fugleinfluenzaen i 2009
- H10N7 Fugleinfluenzaen i 1979, 1980 og igen i 2014
- Virus: heste-1 (H7N7) og heste-2 (H3N8) Hesteinfluenzaen i 1956, 2013 og igen i 2014
- (Hesteinfluenzaen heste-H3N8) Hundeinfluenza 1984, 1999, 2003, 2004, 2005, 2006 og igen i 2007
- Influenza A-virus undertype H3N2, stamme A/Fujian/411/2002(H3N2) og influenza A-virus undertype H5N1, stamme A/Fujian (H5N1)Fujian influenza i 2002-2003, 2003–2004, 2004-2005
Influenzavirus B[redigér | rediger kildetekst]

Dette virusmedlem har en virusart: Influenza B. Influenza B inficerer hovedsageligt mennesker.[58] De eneste andre dyr hvortil der har været dokumenteret influenzainfektion er sæler[66] og fritter.[67] Denne art af influenza muterer 2-3 gange langsommere end type A,[68] og er som følge heraf mindre genetisk varierende, hvorved der kun findes en influenza B serotype.[58] Som følge af en mangel på større antigen variation udvikles en mindre grad af immuntitet mod influenza B tidligt i barndommen. Influenza B muterer dog tilstrækkeligt til at vedvarende immunitet ikke er muligt.[69] Den nedsatte antigene ændring kombineret med dets evne til kun at inficere mennesker, (og på den måde hindre at udveksle genetisk materiale med andre virus i andre dyrearter antigent skift) sikrer at pandemier med influenza B virus ikke forekommer.[70]
Influenzavirus C[redigér | rediger kildetekst]
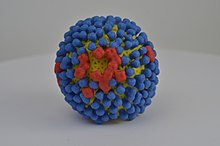

Dette virusmedlem har en virusart: Influenza C som inficerer mennesker, hunde og svin, hvor den nogle gange forårsager mere alvorlige sygdomme og lokale epidemier.[71][72] Influenza C er dog mindre set end de andre typer, og forårsager oftest milde sygdomme blandt børn.[73][74]
Influenzavirus D[redigér | rediger kildetekst]

Dette virusmedlem har en virusart: Influenza D som inficerer mennesker, hunde, katte, heste, fugle, får, geder, køer og svin og også mange andre dyr.
Struktur, egenskaber og serotypenormenklatur[redigér | rediger kildetekst]
Influenzavira A, B, C og D er meget ens i den generelle struktur.[75] Viruspartiklerne er 80-120 nanometer i diameter, og har almindeligvis en sfærisk form eller i visse tilfælde en trådlignende (filamentøs) form.[76][77] De trådlignende former er mest set hos influenza C, som kan danne snorlignende strukturer op til 500 mikrometer lange på overfladen af inficerede celler.[78] Trods de varierende former er viruspartiklerne ens i sammensætningen.[78] Disse udgøres af en kerne som er "kappeklædt" med en lipidmembran (viral envelop). Kernen indeholder viralt RNA-genom og andre virale proteiner, som beskytter RNA'et. Oftest er RNA'et enkelstrenget, men i specielle tilfælde har der været dokumenteret dobbeltstrenget.[77] Genomet forekommer som 7-8 segmenter negativt strenget RNA, hvor hvert stykke indeholder en eller to gener kodende for et genprodukt (protein).[78] For eksempel indeholder Influenza A genomet 11 gener fordelt ud på 8 RNA segmenter, og koder for 11 proteiner: hæmagglutinin (HA), neuraminidase (NA), nukleoprotein (NP), M1, M2, NS1, NS2(NEP: nuklær eksport protein), PA, PB1 (polymerase basic 1), PB1-F2 og PB2.[79]
Hæmagglutinin (HA) og neuraminidase (NA) er to store glykoproteiner på overfladen af viruspartiklerne. HA er et lectin, som giver virus mulighed for at binde sig til bestemte målceller, og frigive det virale genom ind i cellen. NA er involveret i frigivelse af nydannede virus fra inficerede celler ved at kløve sukkerendhederne, der binder den modne virale partikel.[80] Derpå udgør disse målet for en række antivirale medikamenter.[81] Yderligere er disse antigener, hvortil der dannes antistoffer imod. Influenza A virus er klassificeret i serotyper baseret på antistofresponset mod HA og NA. Disse forskellige typer af HA og NA danner grundlaget for H og N-navngivningen som f.eks. H5N1.[82] Der kendes 16 H og 9 N typer, hvor kun H 1,2 og 3 og N 1 og 2 er fundet blandt mennesker.[83]
Replikation[redigér | rediger kildetekst]

Virus kan kun replikere i levende celler.[84] Influenzainfektionen og replikationen er en flertrinet proces: Først skal virus bindes og optages af cellen, hvorefter dets genom skal bringes til et område i cellen, hvor det kan producere nye kopier af de virale proteiner og RNA. Herefter skal disse komponenter samles til virale partikler, hvorved det kan forlade værtscellen.[78]
Influenzavira binder med dets hæmagglutinin til sialinsyresukkerenheder på overfladen af epitelceller lokaliseret i næsen, halsen eller lungerne hos pattedyr og i tarmene hos fugle (Se figur: Stadie 1).[85] Herved optages virus ved endocytose, som medfører, at en del af cellemembran indkapsler virionen og afsnøres til indersiden i et endosom.[86] Det sure miljø i endosomet medfører to ting: Først fusionerer den virale lipidmembran med endosomets membran ved hjælp af hæmagglutinin. Næst baner M2 proteinet, (som er en ionkanal) vej for protoner til at diffundere gennem den virale lipidmembarn og surgøre viruskernen, som opløses og frigiver viralt RNA, kerneproteiner og RNA-afhængig RNA polymerase til cytoplasma (Se figur: Stadie 2).[78][87] M2 ionkanalen blokeres af amantadinmedikamenter, som hindrer infektion.[88]
Disse kerneproteiner og negativt-strenget vRNA danner et kompleks, som transporteres ind i cellekernen, hvor den RNA-afhængige RNA polymerase begynder at transskribere komplementært positivt-strenget vRNA (Stadie 3a og b).[89] Enten vil vRNA eksporteres til cytoplasmaet og translateres (stadie 4), eller forblive i kernen. Nydannede virale proteiner frigives enten fra Golgiapparatet til celleoverfladen (som f.eks. neuramidase og hæmagglutinin, (Stadie 5), eller transporteres tilbage til kernen for at binde vRNA og danne nye virale genomer (stadie 5a). Andre virale proteiner har en lang række forskellige mekanismer i værtscellen, bl.a. at nedbryde cellulært mRNA, og bruge de frigivne nukleotider til vRNA syntese, og også hæmme den almene cellulære translation af mRNA.[90]
Negativt-strenget vRNA (som danner genomet til kommende vira), RNA-afhængig-RNA-polymerase og andre virale proteiner samles til et viron. Hæmagglutinin- og neuraminidase-molekyler klumper sammen i cellemembranen, og danner en "udbuling". vRNA og kerneproteiner forlader cellekernen, og interagerer med denne "membranudbuling" (stadie 6). Den modne virus presses derved gennem membranen, og danner en omkringliggende sfære bestående af værtscellens phoshoplipidmembran hvortil der blev koblet hæmagglutinin og neuramidase (stadie 7).[91] Som i begyndelsen vil virus være fastgjort til cellen via hæmagglutinin. For at frigøre sig kløver neuramidasen sialinsyreenhederne.[85] Efter virusfrigivelse dør cellen.
På grund af manglen på fejllæsende enzymer (en: "proofreading") begår den RNA-afhægige RNA polymerase fejl ved omtrent hvert 10.000. nukleotid, som cirka svarer til længden af influenza vRNA. Derfor har størstedelen af nydannede virus undergået mutationer, som medfører antigent drift, der er en langsom ændring i antigenerne i de virale overfladeglykoproteiner over tid.[92] Inddeling af virusgenomet i 8 segmenter giver mulighed for vRNA udveksling med andre influenzatyper, hvis disse inficerer samme celle. Dette medfører pludselig ændring i de virale genprodukter (antigen skift), som er en pludselig ændring fra et antigen til et andet. Disse store skift giver virus mulighed for at inficere nye værtsarter, og hurtigt undgå den beskyttende immunitet,[82] hvilket er årsagen til pandemiudbrud.
Epidemiologi[redigér | rediger kildetekst]
Sæsoninfluenza[redigér | rediger kildetekst]


Influenzas forekomst topper i vintermånederne, og fordi den nordlige og sydlige halvkugle har vinter på forskellige tidspunkter er der to forskellige influenzasæsoner hvert år. Det er årsagen til at World Health Organization anbefaler to forskellige vacciner hvert år, tilpasset til den nordlige og sydlige halvkugle.[93]
En gåde er stadig hvorfor influenza forekommer i bestemte sæsoner og ikke hele året rundt. En mulig forklaring er, at i vintermånederne opholder vi os indendørs og er derved i tæt kontakt, som øger risikoen for person til person smitte. Øget rejsetendens som følge af vinterferierne blandt den nordlige halvkugles populationer, menes også at spille en rolle.[94] En anden faktor er at kolde temperaturer fører til en tørrere luft, som kan dehydrere slimhinderne, og hindre effektiv fjernelse af viruspartikler. Virus overlever også længere på overflader ved lave temperaturer, og aerosol-smitte er højest i kolde omgivelser (under 5 °C) med lav luftfugtighed.[95] Især ser det ud til at lavere luftfugtighed om vinteren, er en betydelig årsag til influenzasmitte i tempereret egne.[96][97] Alligevel ses sæson-afhængige infektioner også i tropiske egne, hvor disse oftest topper i de regnfyldte, våde måneder.[98] Muligvis er sæsoninfluenzaerne også afgjort af kontakt- og ferieforholdene på daginstitutioner som børnehaver og skoler, som det også ses blandt andre børnesygdomme f.eks. mæslinger og kighoste.[99]
En alternativ hypotese til forklaring af influenzas sæsonafhængige forekomst er D-vitamin nivauets indvirken på virusimmunitet.[100] Teorien blev introduceret første gang i 1965 af Robert Edgar Hope-Simpson.[101] Han foreslog at influenzaepidemier i vintermånederne kunne hænge sammen med årstidsændringen af D-vitamin-niveauet, som dannes i huden via UV-lys fra solstråler. Det kunne forklare hvorfor, influenza er hyppigst i vintermånederne og regnsæsonen i tropiske egne, når mennesker opholder sig indendørs og væk fra solen, som danner D-vitamin.
Epidemier og pandemier[redigér | rediger kildetekst]
Influenza forårsages af forskellige influenzavirusarter og deres stammer. Hvert år vil visse stammer uddø, mens andre skaber epidemier og andre pandemier. Almindeligvis forekommer der to influenzasæsoner om året (en for hver halvkugle). Her rapporteres mellem tre og fem millioner alvorlige tilfælde og op til 500.000 dødsfald på verdensplan, som af visse defineres som en årlig influenzaepidemi.[102]
Gennem hvert århundrede forekommer der ca. tre pandemier, hvor en stor del af verdensbefolkningen inficeres og medfører millioner af dødsfald. Et studie estimerede, at hvis en stamme med samme virulens som Den Spanske Syge dukkede op i dag, ville den kunne dræbe mellem 50 og 80 millioner mennesker.[103] Normalt dør 1.000-2.000 danskere om året af influenza.[104][105][106]

Nye influenzavira dannes konstant ved mutation eller genomudveksling.[58] Under replikation og deling kan mutationer forårsage mindre ændringer i hæmagglutinin og neuramidase-antigenerne på overfladen af de nye viruspartikler. Dette fænomen kaldes antigen drift, som langsomt danner nye stammer, indtil der fremkommer en som kan inficere mennesker, der var immun til den før-eksisterende stamme. Denne nye variant erstatter derved den gamle stamme, hvorved den kan spredes i befolkningen og lede til epidemier.[107] Som følge af at stammerne er dannet ud fra drift, og derved stadig vil have visse ligheder med den gamle stamme, er visse mennesker stadig immune overfor dem. Modsat når influenza udveksler gensegmenter, erhverver disse sig fuldkommen nye antigener, f.eks. udveksling mellem en aviær stamme og en human stamme. Dette fænomen betegnes antigen skift. Hvis en human influenzavirus dannes med fuldkommen nye antigener vil alle i populationen være modtagelige overfor denne, og det vil give ukontrollerbare spredningsmuligheder, som kan lede til pandemier.[108] I modsætning til denne pandemiteori er en alternativ hypotese blevet opsat, der postulerer at periodiske pandemier skyldes ændringer i populationens immunitet overfor virusstammerne frem for disses antigen drift og skift egenskaber.[109]

Blandt befolkningen spredes influenzaepidemier hurtigt og er svære at kontrollere. De fleste virusstammer er ikke betydeligt infektiøse, og hvert inficeret individ vil cirka smitte en eller to andre, (reproduktionstallet for influenza ligger generelt på 1,4). Generationstiden (tiden fra en person bliver inficeret til vedkommende smitter den næste) for influenza er rimelig kort (cirka to dage). Den korte generationstid betyder, at influenzaepidemier topper omkring 2 måneder, og udbrænder efter 3 måneder: Beslutningen om indgriben i en mulig influenzaepidemi skal derfor træffes tidligt i forløbet, og er derved ofte baseret på ufuldstændig data. Et andet problem er at inficerede individer bliver smittedygtige før deres symptomer opstår, hvorved karantæne af syge individer ikke har nogen forebyggende effekt.[110] Gennemsnitligt plejer virusspredning at toppe på 2. dagen, mens symptomerne topper på 3. dagen.[17]
Referencer[redigér | rediger kildetekst]
Se også[redigér | rediger kildetekst]
- Coronavirus
- Fugleinfluenza (aviær influenza)
- RNA-vaccine
Eksterne henvisninger[redigér | rediger kildetekst]
- Influenzavirus. Model med molekylær beskrivelse Arkiveret 5. marts 2016 hos Wayback Machine
- Mystery of 1918 Pandemic Flu Virus Solved by UA Researchers. UANews
- Flu may be spread just by breathing University of Maryland på sciencedaily.com januar 2018
Fodnoter[redigér | rediger kildetekst]
- ^ Influenzaens ABC. Videnskab.dk 2009
- ^ a b c "Influenza: Viral Infections: Merck Manual Home Edition". www.merck.com. Hentet 2008-03-15.
- ^ a b Eccles, R (2005). "Understanding the symptoms of the common cold and influenza". Lancet Infect Dis. 5 (11): 718-25. doi:10.1016/S1473-3099(05)70270-X. PMID 16253889.
- ^ Seasonal Flu vs. Stomach Flu Arkiveret 7. juli 2011 hos Wayback Machine by Kristina Duda, R.N.; hentet 12. marts 2007 (Website: "About, Inc., A part of The New York Times Company")
- ^ COLLECTION 19 MAY 2020 Editor's choice: Influenza. Nature Reviews
- ^ Reid AH, Fanning TG, Hultin JV, Taubenberger JK (1999). "Origin and evolution of the 1918 "Spanish" influenza virus hemagglutinin gene". Proc. Natl. Acad. Sci. U.S.A. 96 (4): 1651-6. doi:10.1073/pnas.96.4.1651. PMID 9990079.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Mase M, Tanimura N, Imada T, Okamatsu M, Tsukamoto K, Yamaguchi S (december 2006). "Recent H5N1 avian influenza A virus increases rapidly in virulence to mice after a single passage in mice". J Gen Virol. 87 (Pt 12): 3655-9. doi:10.1099/vir.0.81843-0. PMID 17098982. Arkiveret fra originalen 10. oktober 2008. Hentet 17. januar 2009.
To prepare the original virus stock for this study, virus was propagated once in the allantoic cavity of embryonated eggs at 37 °C for 1–2 days and then stored at –80 °C until use.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Suarez, D; Spackman, E; Senne, D; Bulaga, L; Welsch, A; Froberg, K (2003). "The effect of various disinfectants on detection of avian influenza virus by real time RT-PCR". Avian Dis. 47 (3 Suppl): 1091-5. PMID 14575118.
- ^ Avian Influenza (Bird Flu) Arkiveret 17. juni 2013 hos Wayback Machine: Implications for Human Disease. Physical characteristics of influenza A viruses. UMN CIDRAP.
- ^ Flu viruses 'can live for decades' on ice, NZ Herald, 30. november 2006.
- ^ "Avian influenza ("bird flu") fact sheet". WHO. februar 2006. Hentet 2006-10-20.
- ^ WHO position paper: influenza vaccines WHO weekly Epidemiological Record 19 August 2005, vol. 80, 33, pp. 277–288.
- ^ Villegas, P (1998). "Viral diseases of the respiratory system". Poult Sci. 77 (8): 1143-5. PMID 9706079.
- ^ Horwood F, Macfarlane J (oktober 2002). "Pneumococcal and influenza vaccination: current situation and future prospects". Thorax. 57 (Suppl 2): II24-II30. PMC 1766003. PMID 12364707.
- ^ a b c d Call S, Vollenweider M, Hornung C, Simel D, McKinney W (2005). "Does this patient have influenza?". JAMA. 293 (8): 987-97. doi:10.1001/jama.293.8.987. PMID 15728170.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Centers for Disease Control and Prevention > Influenza Symptoms Sidst opdateret 16. november 2007. Hentet 28. april 2009.
- ^ a b Time Lines of Infection and Disease in Human Influenza: A Review of Volunteer Challenge Studies, American Journal of Epidemiology, Carrat, Vergu, Ferguson, et al., 167 (7): 775–785, 2008. " . . . In almost all studies, participants were individually confined for 1 week. . . " See especially Figure 5 which shows that virus shedding tends to peak on day 2 whereas symptoms tend to peak on day 3.
- ^ Suzuki E, Ichihara K, Johnson AM (januar 2007). "Natural course of fever during influenza virus infection in children". Clin Pediatr (Phila). 46 (1): 76-9. doi:10.1177/0009922806289588. PMID 17164515.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Influenza • Symptomer, varighed og vaccine • Behandling online • euroClinix®
- ^ Næseblod (Epistaxis)
- ^ Øjenbetændelse
- ^ a b Lungebetændelse: Læs mere om symptomer og få gode råd | Apopro.dk
- ^ Lungebetændelse – Læs om symptomer og behandling
- ^ Lungebetændelse (Pneumoni)
- ^ "Arkiveret kopi". Arkiveret fra originalen 20. september 2022. Hentet 16. september 2022.
- ^ Lungebetændelse - Find information på Medicin.dk
- ^ Lungebetændelse (pneumoni) | Lungeforeningen
- ^ Vaccination mod influenza og lungebetændelse | Lungeforeningen
- ^ a b Richards S (2005). "Flu blues". Nurs Stand. 20 (8): 26-7. PMID 16295596.
- ^ Heikkinen T (juli 2006). "Influenza in children". Acta Paediatr. 95 (7): 778-84. doi:10.1080/08035250600612272. PMID 16801171.
- ^ Kerr AA, McQuillin J, Downham MA, Gardner PS (1975). "Gastric 'flu influenza B causing abdominal symptoms in children". Lancet. 1 (7902): 291-5. doi:10.1016/S0140-6736(75)91205-2. PMID 46444.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Hui DS (marts 2008). "Review of clinical symptoms and spectrum in humans with influenza A/H5N1 infection". Respirology. 13 Suppl 1: S10-3. doi:10.1111/j.1440-1843.2008.01247.x. PMID 18366521.
- ^ Hospitalized Patients with 2009 H1N1 Influenza in the United States, April–June 2009, New England Journal of Medicine, Jain, Kamimoto, et al., 12 November 2009.
- ^ Transcript of virtual press conference with Gregory Hartl, Spokesperson for H1N1, and Dr Nikki Shindo, Medical Officer, Global Influenza Programme, World Health Organization, 12 November 2009.
- ^ Report Finds Swine Flu Has Killed 36 Children, New York Times, DENISE GRADY, 3. september 2009.
- ^ Influenza A (H1N1) - information til gravide
- ^ Forkølelse eller influenza | Panodil
- ^ Ti myter om influenza og forkølelse
- ^ Blærebetændelse – læs om symptomerne her | Webapoteket
- ^ Kawaoka Y (editor) (2006). Influenza Virology: Current Topics. Caister Academic Press. ISBN 978-1-904455-06-6.
{{cite book}}:|author=har et generisk navn (hjælp) - ^ Substantial effect of phytochemical constituents against the pandemic disease influenza—a review | Future Journal of Pharmaceutical Sciences | Full Text
- ^ Types of Influenza Viruses | CDC
- ^ https://www.cdc.gov/flu/about/viruses/types.htm
- ^ Vaccines | Free Full-Text | The Power of First Impressions: Can Influenza Imprinting during Infancy Inform Vaccine Design?
- ^ a b JCM | Free Full-Text | Emerging Influenza D Virus Threat: What We Know so Far!
- ^ "The Continual Threat of Influenza Virus Infections at the Human-Animal Interface | Duke One Health". Arkiveret fra originalen 20. september 2022. Hentet 16. september 2022.
- ^ Host and viral determinants of influenza A virus species specificity | Nature Reviews Microbiology
- ^ Orthomyxoviridae - Wikipedia
- ^ https://www.researchgate.net/figure/The-host-range-for-all-four-types-IAV-IBV-ICV-and-IDV-of-influenza-viruses-The_fig1_333832335/amp
- ^ Viruses | Free Full-Text | Comparing Influenza Virus Biology for Understanding Influenza D Virus
- ^ Influenza D-virus er for første gang påvist i danske kalvebesætninger | LandbrugsAvisen
- ^ Vainionpää R, Hyypiä T (april 1994). "Biology of parainfluenza viruses". Clin. Microbiol. Rev. 7 (2): 265-75. doi:10.1128/CMR.7.2.265. PMC 358320. PMID 8055470.
- ^ Hall CB (juni 2001). "Respiratory syncytial virus and parainfluenza virus". N. Engl. J. Med. 344 (25): 1917-28. doi:10.1056/NEJM200106213442507. PMID 11419430.
- ^ "Arkiveret kopi". Arkiveret fra originalen 20. september 2022. Hentet 16. september 2022.
- ^ "Arkiveret kopi". Arkiveret fra originalen 20. september 2022. Hentet 16. september 2022.
- ^ Inden du fortsætter til YouTube
- ^ Klenk (2008). "Avian Influenza: Molecular Mechanisms of Pathogenesis and Host Range". Animal Viruses: Molecular Biology. Caister Academic Press. ISBN 978-1-904455-22-6.
{{cite book}}: Forkert|display-authors=1(hjælp) - ^ a b c d Hay, A; Gregory, V; Douglas, A; Lin, Y (29. december 2001). "The evolution of human influenza viruses". Philos Trans R Soc Lond B Biol Sci. 356 (1416): 1861-70. doi:10.1098/rstb.2001.0999. PMC 1088562. PMID 11779385.
- ^ Influenza A virus in swine: situation in European countries - Articles - pig333, pig to pork community
- ^ Highly Pathogenic Avian Influenza | Ohioline
- ^ https://www.researchgate.net/figure/Various-reincarnations-of-Influenza-type-A-virus_fig1_315105538/amp
- ^ Fugleinfluenza H5N1 fundet i Danmark
- ^ Økonomiske konsekvenser for dansk fjerkræsektor af udbrud af fugleinfluenza i 2016 og 2017 - Staff at Department of Food and Resource Economics (IFRO)
- ^ Fouchier, RAM; Schneeberger, PM; Rozendaal, FW; Broekman, JM; Kemink, SA; Munster, V; Kuiken, T; Rimmelzwaan, GF; Schutten, M (2004). "Avian influenza A virus (H7N7) associated with human conjunctivitis and a fatal case of acute respiratory distress syndrome" (PDF). Proceedings of the National Academy of Sciences. 101 (5): 1356-61. Bibcode:2004PNAS..101.1356F. doi:10.1073/pnas.0308352100. PMC 337057. PMID 14745020. Arkiveret fra originalen (PDF) 25. januar 2016. Hentet 19. januar 2013.
- ^ "Fugleinfluenza-udbrud i Danmark". Arkiveret fra originalen 20. september 2022. Hentet 16. september 2022.
- ^ Osterhaus, A; Rimmelzwaan, G; Martina, B; Bestebroer, T; Fouchier, R (2000). "Influenza B virus in seals". Science. 288 (5468): 1051-3. Bibcode:2000Sci...288.1051O. doi:10.1126/science.288.5468.1051. PMID 10807575.
- ^ Jakeman KJ, Tisdale M, Russell S, Leone A, Sweet C (august 1994). "Efficacy of 2'-deoxy-2'-fluororibosides against influenza A and B viruses in ferrets". Antimicrob. Agents Chemother. 38 (8): 1864-7. PMC 284652. PMID 7986023.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Nobusawa, E; Sato, K (april 2006). "Comparison of the mutation rates of human influenza A and B viruses". J Virol. 80 (7): 3675-8. doi:10.1128/JVI.80.7.3675-3678.2006. PMC 1440390. PMID 16537638.
- ^ R, Webster; Bean, W; Gorman, O; Chambers, T; Kawaoka, Y (1992). "Evolution and ecology of influenza A viruses". Microbiol Rev. 56 (1): 152-79. PMC 372859. PMID 1579108.
- ^ Zambon, M (november 1999). "Epidemiology and pathogenesis of influenza" (PDF). J Antimicrob Chemother. 44 Suppl B (90002): 3-9. doi:10.1093/jac/44.suppl_2.3. PMID 10877456.
- ^ Matsuzaki, Y; Sugawara K; Mizuta K; Tsuchiya E; Muraki Y; Hongo S; Suzuki H; Nakamura K (2002). "Antigenic and genetic characterization of influenza C viruses which caused two outbreaks in Yamagata City, Japan, in 1996 and 1998". J Clin Microbiol. 40 (2): 422-9. doi:10.1128/JCM.40.2.422-429.2002. PMC 153379. PMID 11825952.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Taubenberger, JK; Morens, DM (2008). "The pathology of influenza virus infections". Annu Rev Pathol. 3: 499-522. doi:10.1146/annurev.pathmechdis.3.121806.154316. PMC 2504709. PMID 18039138.
- ^ Matsuzaki, Y; Katsushima N; Nagai Y; Shoji M; Itagaki T; Sakamoto M; Kitaoka S; Mizuta K; Nishimura H (1. maj 2006). "Clinical features of influenza C virus infection in children". J Infect Dis. 193 (9): 1229-35. doi:10.1086/502973. PMID 16586359.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Katagiri, S; Ohizumi, A; Homma, M (juli 1983). "An outbreak of type C influenza in a children's home". J Infect Dis. 148 (1): 51-6. doi:10.1093/infdis/148.1.51. PMID 6309999.
- ^ International Committee on Taxonomy of Viruses descriptions of:Orthomyxoviridae Arkiveret 2. oktober 2006 hos Wayback Machine,Influenzavirus B Arkiveret 6. oktober 2007 hos Wayback Machine and Influenzavirus C Arkiveret 31. december 2009 hos Wayback Machine
- ^ International Committee on Taxonomy of Viruses. "The Universal Virus Database, version 4: Influenza A". Arkiveret fra originalen 13. januar 2010. Hentet 20. januar 2013.
- ^ a b Lamb RA, Choppin PW (1983). "The gene structure and replication of influenza virus". Annu. Rev. Biochem. 52: 467-506. doi:10.1146/annurev.bi.52.070183.002343. PMID 6351727.
- ^ a b c d e Bouvier NM, Palese P (september 2008). "The biology of influenza viruses". Vaccine. 26 Suppl 4: D49-53. doi:10.1016/j.vaccine.2008.07.039. PMC 3074182. PMID 19230160.
- ^ Ghedin, E; Sengamalay, NA; Shumway, M; Zaborsky, J; Feldblyum, T; Subbu, V; Spiro, DJ; Sitz, J; Koo, H (oktober 2005). "Large-scale sequencing of human influenza reveals the dynamic nature of viral genome evolution". Nature. 437 (7062): 1162-6. Bibcode:2005Natur.437.1162G. doi:10.1038/nature04239. PMID 16208317.
- ^ Suzuki, Y (2005). "Sialobiology of influenza: molecular mechanism of host range variation of influenza viruses". Biol Pharm Bull. 28 (3): 399-408. doi:10.1248/bpb.28.399. PMID 15744059. Arkiveret fra originalen 12. januar 2009. Hentet 20. januar 2013.
- ^ Wilson, J; von Itzstein, M (juli 2003). "Recent strategies in the search for new anti-influenza therapies". Curr Drug Targets. 4 (5): 389-408. doi:10.2174/1389450033491019. PMID 12816348.
- ^ a b Hilleman, M (19. august 2002). "Realities and enigmas of human viral influenza: pathogenesis, epidemiology and control". Vaccine. 20 (25-26): 3068-87. doi:10.1016/S0264-410X(02)00254-2. PMID 12163258.
- ^ Lynch JP, Walsh EE (april 2007). "Influenza: evolving strategies in treatment and prevention". Semin Respir Crit Care Med. 28 (2): 144-58. doi:10.1055/s-2007-976487. PMID 17458769.
- ^ Smith AE, Helenius A (april 2004). "How viruses enter animal cells". Science. 304 (5668): 237-42. Bibcode:2004Sci...304..237S. doi:10.1126/science.1094823. PMID 15073366.
- ^ a b Wagner, R; Matrosovich, M; Klenk, H (maj-juni 2002). "Functional balance between haemagglutinin and neuraminidase in influenza virus infections". Rev Med Virol. 12 (3): 159-66. doi:10.1002/rmv.352. PMID 11987141.
{{cite journal}}: CS1-vedligeholdelse: Dato-format (link) - ^ Steinhauer DA (maj 1999). "Role of hemagglutinin cleavage for the pathogenicity of influenza virus". Virology. 258 (1): 1-20. doi:10.1006/viro.1999.9716. PMID 10329563.
- ^ Lakadamyali, M; Rust, M; Babcock, H; Zhuang, X (5. august 2003). "Visualizing infection of individual influenza viruses". Proc Natl Acad Sci USA. 100 (16): 9280-5. Bibcode:2003PNAS..100.9280L. doi:10.1073/pnas.0832269100. PMC 170909. PMID 12883000.
- ^ Pinto LH, Lamb RA (april 2006). "The M2 proton channels of influenza A and B viruses". J. Biol. Chem. 281 (14): 8997-9000. doi:10.1074/jbc.R500020200. PMID 16407184.
- ^ Cros, J; Palese, P (september 2003). "Trafficking of viral genomic RNA into and out of the nucleus: influenza, Thogoto and Borna disease viruses". Virus Res. 95 (1-2): 3-12. doi:10.1016/S0168-1702(03)00159-X. PMID 12921991.
- ^ Kash, J; Goodman, A; Korth, M; Katze, M (juli 2006). "Hijacking of the host-cell response and translational control during influenza virus infection". Virus Res. 119 (1): 111-20. doi:10.1016/j.virusres.2005.10.013. PMID 16630668.
- ^ Nayak, D; Hui, E; Barman, S (december 2004). "Assembly and budding of influenza virus". Virus Res. 106 (2): 147-65. doi:10.1016/j.virusres.2004.08.012. PMID 15567494.
- ^ Drake, J (1. maj 1993). "Rates of spontaneous mutation among RNA viruses". Proc Natl Acad Sci USA. 90 (9): 4171-5. Bibcode:1993PNAS...90.4171D. doi:10.1073/pnas.90.9.4171. PMC 46468. PMID 8387212.
- ^ Recommended composition of influenza virus vaccines for use in the 2006–2007 influenza season WHO report 14. februar 2006. Hentet 19. oktober 2006.
- ^ Weather and the Flu Season NPR Day to Day, 17 December 2003. Retrieved, 19 October 2006
- ^ Lowen, AC; Mubareka, S; Steel, J; Palese, P (oktober 2007). "Influenza virus transmission is dependent on relative humidity and temperature" (PDF). PLoS Pathogens. 3 (10): 1470-6. doi:10.1371/journal.ppat.0030151. PMC 2034399. PMID 17953482. (Webside ikke længere tilgængelig)
- ^ Shaman J, Kohn M (marts 2009). "Absolute humidity modulates influenza survival, transmission, and seasonality". Proc. Natl. Acad. Sci. U.S.A. 106 (9): 3243-8. Bibcode:2009PNAS..106.3243S. doi:10.1073/pnas.0806852106. PMC 2651255. PMID 19204283.
- ^ Shaman J, Pitzer VE, Viboud C, Grenfell BT, Lipsitch M (februar 2010). Ferguson, Neil M (red.). "Absolute humidity and the seasonal onset of influenza in the continental United States". PLoS Biol. 8 (2): e1000316. doi:10.1371/journal.pbio.1000316. PMC 2826374. PMID 20186267.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ Shek, LP; Lee, BW (2003). "Epidemiology and seasonality of respiratory tract virus infections in the tropics". Paediatric respiratory reviews. 4 (2): 105-11. doi:10.1016/S1526-0542(03)00024-1. PMID 12758047.
- ^ Dushoff, J; Plotkin, JB; Levin, SA; Earn, DJ (2004). "Dynamical resonance can account for seasonality of influenza epidemics". Proceedings of the National Academy of Sciences of the United States of America. 101 (48): 16915-6. Bibcode:2004PNAS..10116915D. doi:10.1073/pnas.0407293101. PMC 534740. PMID 15557003.
- ^ Cannell, J; Vieth R; Umhau J; Holick M; Grant W; Madronich S; Garland C; Giovannucci E (2006). "Epidemic influenza and vitamin D". Epidemiol Infect. 134 (6): 1129-40. doi:10.1017/S0950268806007175. PMC 2870528. PMID 16959053.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ HOPE-SIMPSON, R (1965). "The nature of herpes zoster: a long-term study and a new hypothesis". Proc R Soc Med. 58: 9-20. PMC 1898279. PMID 14267505.
- ^ Influenza WHO Fact sheet No. 211 revised marts 2003. Hentet 22. oktober 2006.
- ^ Murray CJ, Lopez AD, Chin B, Feehan D, Hill KH (december 2006). "Estimation of potential global pandemic influenza mortality on the basis of vital registry data from the 1918–20 pandemic: a quantitative analysis". Lancet. 368 (9554): 2211-8. doi:10.1016/S0140-6736(06)69895-4. PMID 17189032.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ "Influenza". www.sst.dk. Sundhedsstyrelsen. 8. juli 2019. Arkiveret fra originalen 30. marts 2020. Hentet 11. marts 2020.
- ^ "Dødsfald". www.dst.dk. Danmarks Statistik.
- ^ Dahl, Uffe (28. februar 2020). "Hvor mange danskere dør af influenza om året?". Newsbreak.dk. Arkiveret fra originalen 29. februar 2020. Hentet 11. marts 2020.
- ^ Wolf, Yuri I; Viboud, C; Holmes, EC; Koonin, EV; Lipman, DJ (2006). "Long intervals of stasis punctuated by bursts of positive selection in the seasonal evolution of influenza A virus". Biol Direct. 1 (1): 34. doi:10.1186/1745-6150-1-34. PMC 1647279. PMID 17067369.
- ^ Parrish, C; Kawaoka, Y (2005). "The origins of new pandemic viruses: the acquisition of new host ranges by canine parvovirus and influenza A viruses". Annual Rev Microbiol. 59: 553-86. doi:10.1146/annurev.micro.59.030804.121059. PMID 16153179.
- ^ Recker M, Pybus OG, Nee S, Gupta S (2007). "The generation of influenza outbreaks by a network of host immune responses against a limited set of antigenic types" (PDF). Proc Natl Acad Sci U S A. 104 (18): 7711-16. Bibcode:2007PNAS..104.7711R. doi:10.1073/pnas.0702154104. PMC 1855915. PMID 17460037. Arkiveret fra originalen (PDF) 24. september 2015. Hentet 24. januar 2013.
{{cite journal}}: CS1-vedligeholdelse: Flere navne: authors list (link) - ^ a b Ferguson, NM; Cummings, DA; Cauchemez, S; Fraser, C; Riley, S; Meeyai, A; Iamsirithaworn, S; Burke, DS (2005). "Strategies for containing an emerging influenza pandemic in Southeast Asia". Nature. 437 (7056): 209-14. Bibcode:2005Natur.437..209F. doi:10.1038/nature04017. PMID 16079797.
